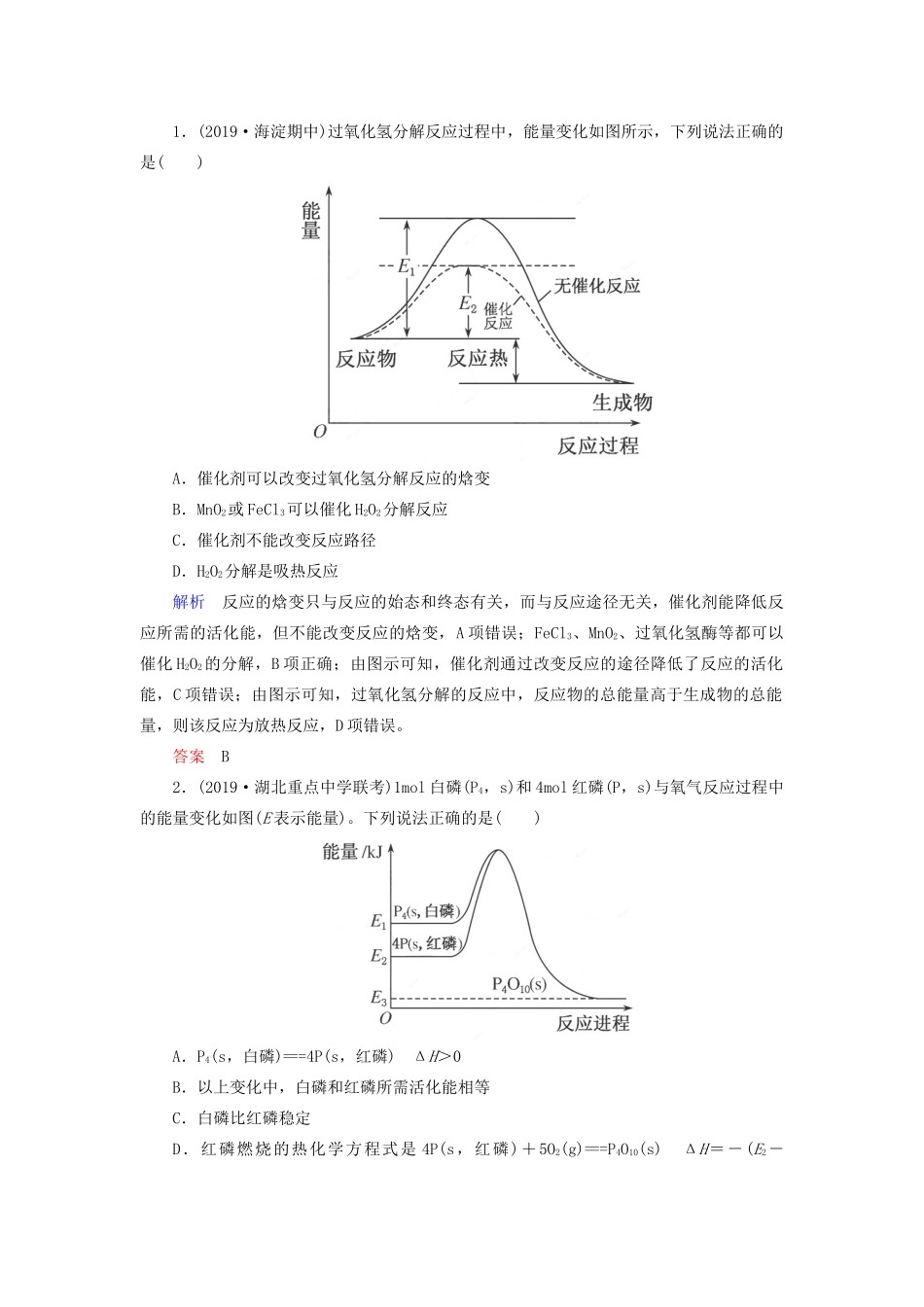
专题6化学反应与能量考|情|分|析考点1反应热的相关概念及热化学方程式的书写核|心|回|顾1.理解化学反应热效应的两种角度(1)从微观的角度说,是旧化学键断裂吸收的能量与新化学键形成放出的能量的差值,如图所示:a表示旧化学键断裂吸收的能量;b表示新化学键形成放出的能量;c表示反应热。(2)从宏观的角度说,是反应物自身的能量与生成物能量的差值,在上图中:a表示活化能;b表示活化分子结合成生成物所释放的能量;c表示反应热。2.反应热的量化参数——键能反应热与键能的关系反应热:ΔH=E1-E2或ΔH=E4-E3,即ΔH等于反应物的键能总和减去生成物的键能总和,或生成物具有的总能量减去反应物具有的总能量。3.对燃烧热和中和热的理解(1)燃烧热:在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量。单位:kJ·mol-1。需注意:①燃烧热是以1mol纯物质完全燃烧生成稳定的氧化物放出的热量来定义的,因此在书写燃烧热的热化学方程式时,一般以燃烧1mol纯物质为标准来配平其余物质的化学计量数;②燃烧产物必须是稳定的氧化物,如C→CO2、H2→H2O(l)等。(2)中和热:在稀溶液中,强酸跟强碱发生中和反应生成1mol液态H2O时的反应热。需注意:①稀溶液是指物质溶于大量水中;②中和热不包括离子在水溶液中的生成热、物质的溶解热、电解质电离时的热效应;③中和反应的实质是H+和OH-化合生成H2O,即H+(aq)+OH-(aq)===H2O(l)ΔH=-57.3kJ·mol-1。4.热化学方程式的书写(1)ΔH的符号和单位若为放热反应,ΔH为“-”;若为吸热反应,ΔH为“+”。ΔH的单位为kJ·mol-1。(2)热化学方程式中的化学计量数热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物质的量,并不表示物质的分子数或原子数。因此化学计量数可以是整数,也可以是分数。(3)物质的聚集状态反应物和产物的聚集状态不同,反应热ΔH不同。因此,必须注明物质的聚集状态才能完整地体现出热化学方程式的意义。气体用“g”,液体用“l”,固体用“s”,溶液用“aq”。热化学方程式中不用“↑”和“↓”以及“点燃”“加热”等条件。(4)ΔH的数值与符号由于ΔH与反应完成的物质的量有关,所以ΔH必须与热化学方程式中化学式前面的化学计量数相对应,如果化学计量数加倍,则ΔH也要加倍。互为逆反应的反应热数值相等,但符号相反。题|组|训|练题组一有关反应热图象和概念的判断1.(2019·海淀期中)过氧化氢分解反应过程中,能量变化如图所示,下列说法正确的是()A.催化剂可以改变过氧化氢分解反应的焓变B.MnO2或FeCl3可以催化H2O2分解反应C.催化剂不能改变反应路径D.H2O2分解是吸热反应解析反应的焓变只与反应的始态和终态有关,而与反应途径无关,催化剂能降低反应所需的活化能,但不能改变反应的焓变,A项错误;FeCl3、MnO2、过氧化氢酶等都可以催化H2O2的分解,B项正确;由图示可知,催化剂通过改变反应的途径降低了反应的活化能,C项错误;由图示可知,过氧化氢分解的反应中,反应物的总能量高于生成物的总能量,则该反应为放热反应,D项错误。答案B2.(2019·湖北重点中学联考)1mol白磷(P4,s)和4mol红磷(P,s)与氧气反应过程中的能量变化如图(E表示能量)。下列说法正确的是()A.P4(s,白磷)===4P(s,红磷)ΔH>0B.以上变化中,白磷和红磷所需活化能相等C.白磷比红磷稳定D.红磷燃烧的热化学方程式是4P(s,红磷)+5O2(g)===P4O10(s)ΔH=-(E2-E3)kJ·mol-1解析依据图象分析,白磷能量高于红磷,白磷转变为红磷是放热反应,则ΔH<0,A项错误;白磷和红磷所需活化能不相等,红磷所需活化能大,B项错误;白磷能量高于红磷,能量越低越稳定,则红磷稳定,C项错误;红磷燃烧是放热反应,则反应的热化学方程式为4P(s,红磷)+5O2(g)===P4O10(s)ΔH=-(E2-E3)kJ·mol-1,D项正确。答案D3.H2和I2在一定条件下能发生反应:H2(g)+I2(g)2HI(g)ΔH=-akJ·mol-1已知:ⒽⒽ――→Ⓗ+ⒽⒾⒾ――→Ⓘ+Ⓘ(a、b、c均大于零),下列说法不正确的是()A.反应物的总能量高于生成物的总能量B.断开2molH—I键所需能量约为(c+b+a)kJC.断开1molH—H键和1molI—I键所需能量大于断开2mol...