第21讲化学能转化为电能——电池目标要求1
以原电池为例认识化学能可以转化为电能,从氧化还原反应的角度认识原电池的工作原理,能设计简单的原电池
体会提高燃料的燃烧效率、开发高纯清洁燃料和研制新型电池的重要性
认识化学能与电能相互转化的实际意义及其重要应用,了解原电池及其常见化学电源的工作原理;能利用相关信息分析化学电源的工作原理,开发新型电池
了解金属发生电化学腐蚀的本质,知道金属腐蚀的危害,能利用电化学原理解释金属腐蚀现象,选择设计防腐措施
1.概念和反应本质原电池是把化学能转化为电能的装置,其反应本质是氧化还原反应
2.构成条件(1)一看反应:看是否有能自发进行的氧化还原反应发生(一般是活泼性强的金属与电解质溶液反应)
(2)二看两电极:一般是活泼性不同的两电极
(3)三看是否形成闭合回路,形成闭合回路需三个条件:①电解质溶液;②两电极直接或间接接触;③两电极插入电解质溶液中
理解应用在如图所示的4个装置中,不能形成原电池的是______(填序号),并指出原因______________________________________________________________________________________
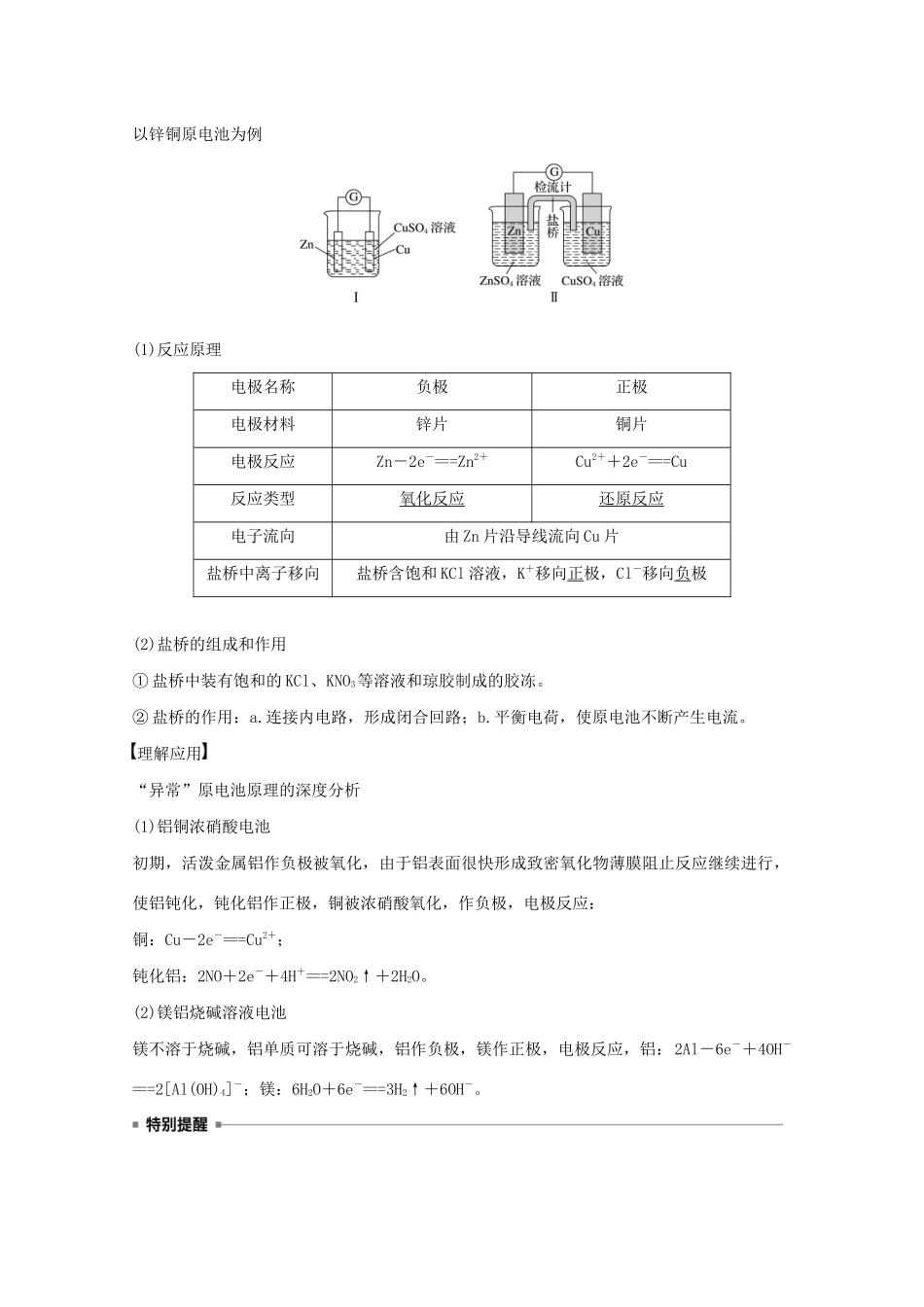
答案①④①中酒精是非电解质;④中未形成闭合回路3.工作原理以锌铜原电池为例(1)反应原理电极名称负极正极电极材料锌片铜片电极反应Zn-2e-===Zn2+Cu2++2e-===Cu反应类型氧化反应还原反应电子流向由Zn片沿导线流向Cu片盐桥中离子移向盐桥含饱和KCl溶液,K+移向正极,Cl-移向负极(2)盐桥的组成和作用①盐桥中装有饱和的KCl、KNO3等溶液和琼胶制成的胶冻
②盐桥的作用:a
连接内电路,形成闭合回路;b
平衡电荷,使原电池不断产生电流
理解应用“异常”原电池原理的深度分析(1)铝铜浓硝酸电池初期,活泼金属铝作负极