第20讲电能转化为化学能——电解目标要求了解电解池的工作原理,能设计简单的电解池
1.电解和电解池(1)电解:在电流作用下,电解质在两个电极上分别发生氧化反应和还原反应的过程
(2)电解池:电能转化为化学能的装置
(3)电解池的构成①有与电源相连的两个电极
②电解质溶液(或熔融电解质)
③形成闭合回路
2.电解池的工作原理(以惰性电极电解CuCl2溶液为例)总反应离子方程式:Cu2++2Cl-=====Cu+Cl2↑
特别提醒:电子和离子的移动遵循“电子不下水,离子不上线”
3.阴阳两极上放电顺序(1)阴极:(与电极材料无关)
氧化性强的先放电,放电顺序:(2)阳极:若是活性电极作阳极,则活性电极首先失电子,发生氧化反应
若是惰性电极作阳极,放电顺序为注意①阴极不管是什么材料,电极本身都不反应,一定是溶液(或熔融电解质)中的阳离子放电
②最常用、最重要的放电顺序为阳极:Cl->OH-;阴极:Ag+>Cu2+>H+
③电解水溶液时,K+~Al3+不可能在阴极放电
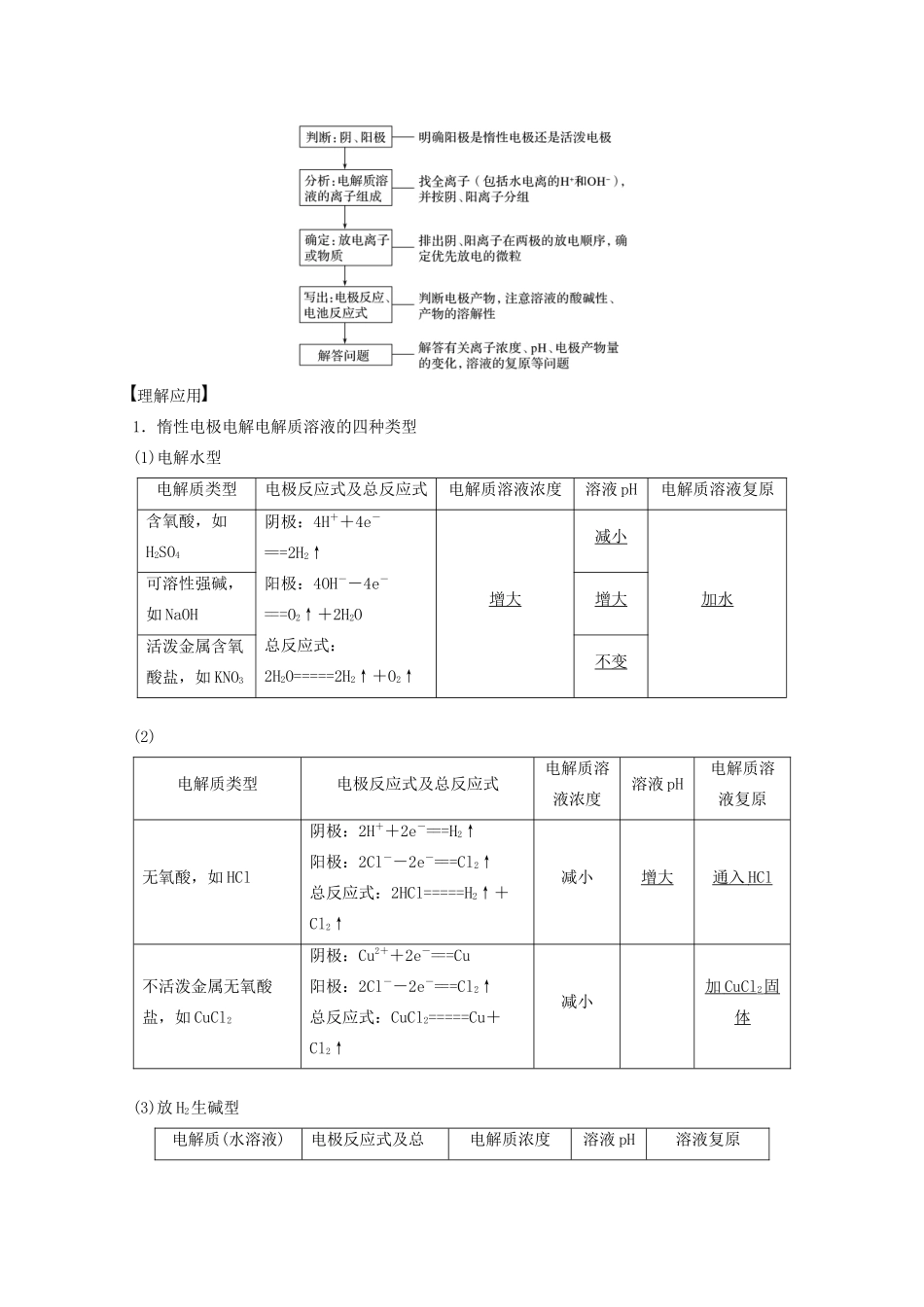
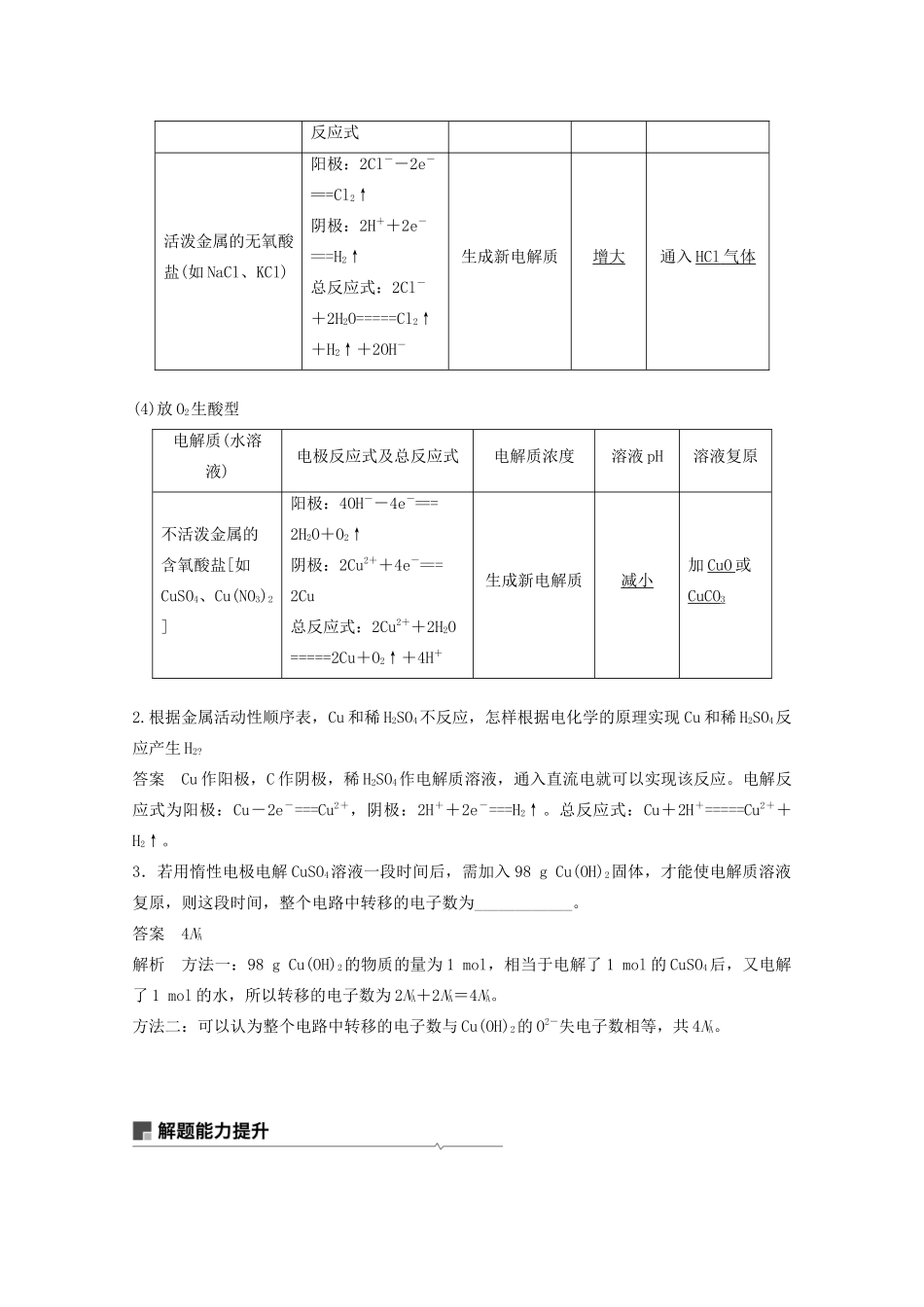
4.分析电解过程的思维程序理解应用1.惰性电极电解电解质溶液的四种类型(1)电解水型电解质类型电极反应式及总反应式电解质溶液浓度溶液pH电解质溶液复原含氧酸,如H2SO4阴极:4H++4e-===2H2↑阳极:4OH--4e-===O2↑+2H2O总反应式:2H2O=====2H2↑+O2↑增大减小加水可溶性强碱,如NaOH增大活泼金属含氧酸盐,如KNO3不变(2)电解质类型电极反应式及总反应式电解质溶液浓度溶液pH电解质溶液复原无氧酸,如HCl阴极:2H++2e-===H2↑阳极:2Cl--2e-===Cl2↑总反应式:2HCl=====H2↑+Cl2↑减小增大通入HCl不活泼金属无氧酸盐,如CuCl2阴极:Cu2++2e-===Cu阳极:2Cl--2e-===Cl2↑总反应式:CuCl2=====Cu+Cl2↑减