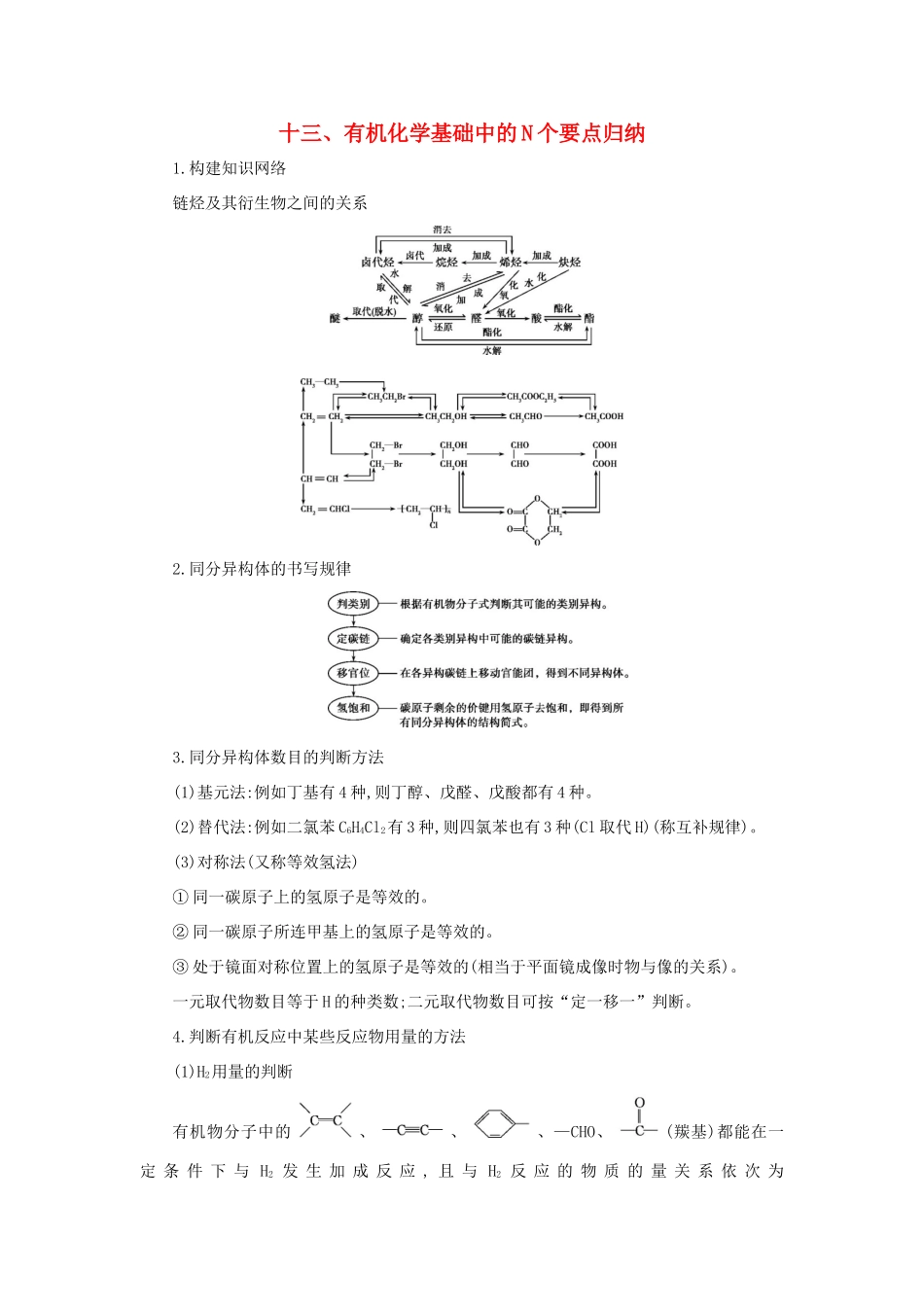
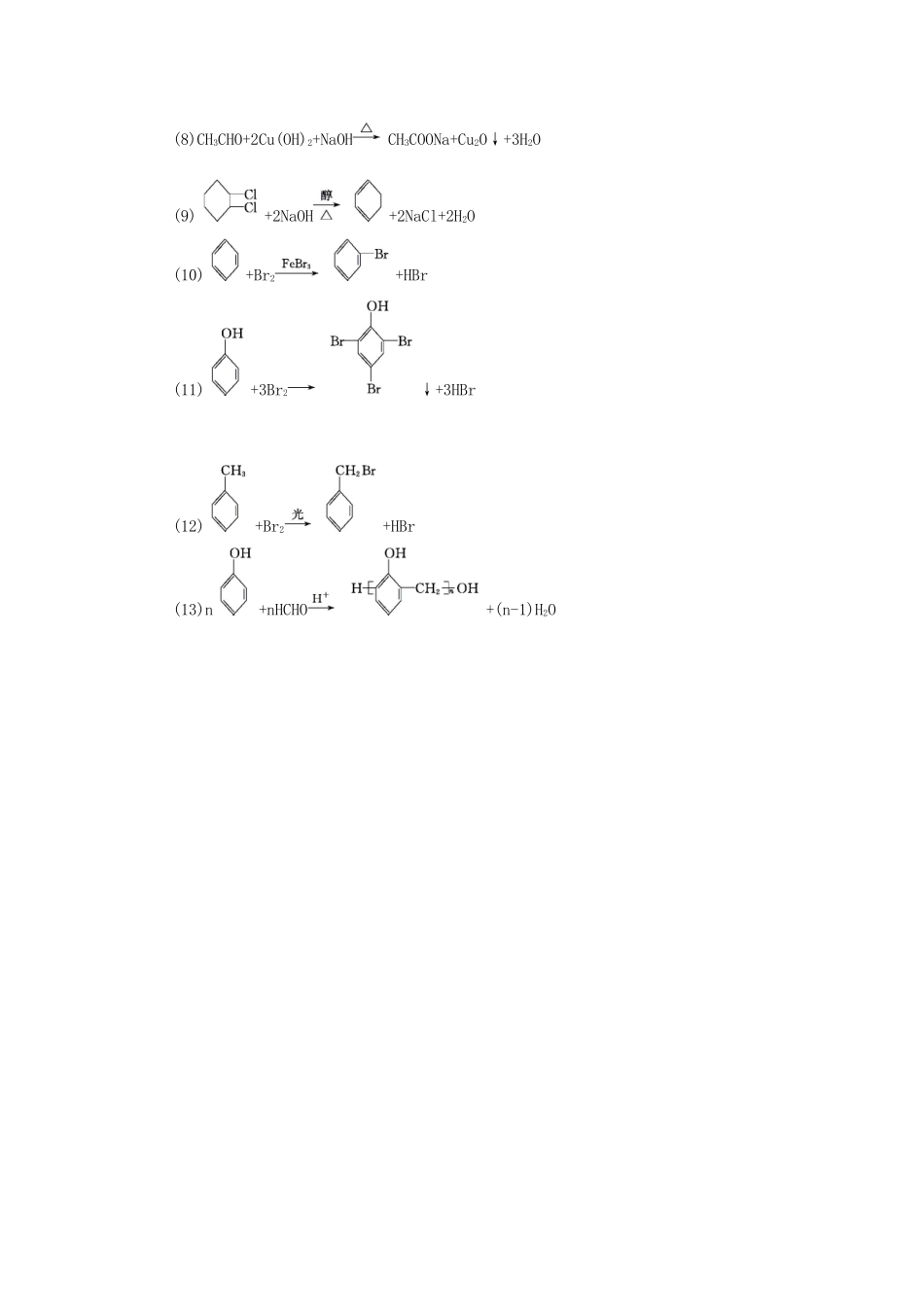
十三、有机化学基础中的N个要点归纳1.构建知识网络链烃及其衍生物之间的关系2.同分异构体的书写规律3.同分异构体数目的判断方法(1)基元法:例如丁基有4种,则丁醇、戊醛、戊酸都有4种。(2)替代法:例如二氯苯C6H4Cl2有3种,则四氯苯也有3种(Cl取代H)(称互补规律)。(3)对称法(又称等效氢法)①同一碳原子上的氢原子是等效的。②同一碳原子所连甲基上的氢原子是等效的。③处于镜面对称位置上的氢原子是等效的(相当于平面镜成像时物与像的关系)。一元取代物数目等于H的种类数;二元取代物数目可按“定一移一”判断。4.判断有机反应中某些反应物用量的方法(1)H2用量的判断有机物分子中的、、、—CHO、(羰基)都能在一定条件下与H2发生加成反应,且与H2反应的物质的量关系依次为1∶1、1∶2、1∶3、1∶1、1∶1。特别注意—COOH、—COOR(酯基)中的CO通常不与H2发生加成反应。(2)NaOH用量的判断—COOH、—OH(酚羟基)、酯类物质、卤代烃能与NaOH溶液发生反应,特别要注意,水解产物能否与NaOH发生反应,如1mol与NaOH溶液发生反应时最多消耗3molNaOH。(3)Br2用量的判断烷烃(光照下1molBr2可取代1molH原子)、苯(FeBr3催化下1molBr2可取代1molH原子)、酚类(1molBr2可取代与—OH处于邻、对位上的1molH原子)、(1mol双键可与1molBr2发生加成反应)、(1mol三键可与2molBr2发生加成反应)。5.熟记重要反应(1)CH3CH2Cl+NaOHCH2CH2↑+NaCl+H2O(2)CH3CH2OHCH2CH2↑+H2O↑(3)2CH3CH2OH+O22CH3CHO+2H2O(4)CH3COOH+CH3CH2OHCH3COOC2H5+H2O(5)OHC—CHO+O2HOOC—COOH(6)nHOCH2—CH2OH+nHOOC—COOH+(2n-1)H2O(7)CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag↓+3NH3+H2O(8)CH3CHO+2Cu(OH)2+NaOHCH3COONa+Cu2O↓+3H2O(9)+2NaOH+2NaCl+2H2O(10)+Br2+HBr(11)+3Br2↓+3HBr(12)+Br2+HBr(13)n+nHCHO+(n-1)H2O