第6课常见的酸与碱学科网中考考纲具体要求1
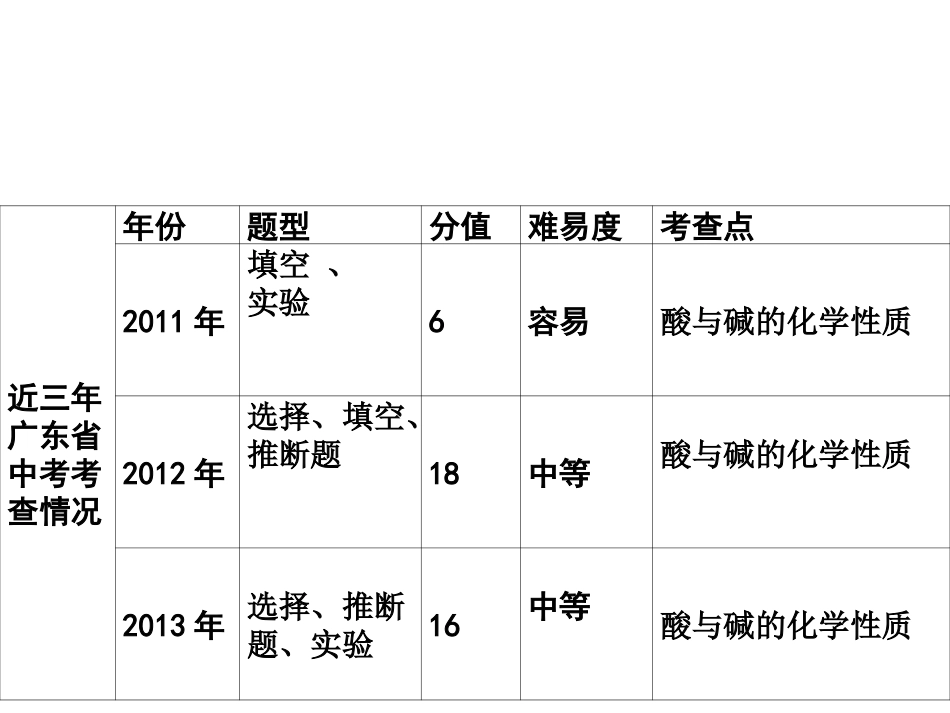
常见的酸与碱的主要性质和用途(认识)2.酸碱的腐蚀性(知道)3.常见酸碱的稀释方法(独立操作)4.用酸碱指示剂和pH试纸检验溶液酸碱性的方法(独立操作)5.酸碱性对人体健康和农作物生长的影响(认识)近三年广东省中考考查情况年份题型分值难易度考查点2011年填空、实验6容易酸与碱的化学性质2012年选择、填空、推断题18中等酸与碱的化学性质2013年选择、推断题、实验16中等酸与碱的化学性质Z
K一、酸的性质(请对应完成后面练习1~11题)1.物理性质浓盐酸浓硫酸盐酸是HCl气体溶于水的溶液,浓盐酸有________气味,具有________性,挥发出的氯化氢气体遇空气中的水蒸气形成________________
纯净的浓硫酸是________色黏稠的液体,不易________;浓硫酸具有________性,故可作某些气体的干燥剂
刺激性挥发白雾(或盐酸小液滴)无挥发吸水▲温馨提示:①浓硫酸具有强烈的腐蚀性,溶于水时放出大量的热,故稀释浓硫酸时应酸入水,不能水入酸
②硫酸沾在皮肤上的事故处理方法:立刻用大量的水冲洗,然后涂上3%~5%的碳酸氢钠溶液
③浓硫酸有吸水性、脱水性(化学变化,使物质碳化)、强氧化性(化学变化)
2.化学性质酸有相似的化学性质,是因为它们溶于水后产生的阳离子全部都是________
氢离子(或H+)稀盐酸稀硫酸(1)酸与酸碱指示剂反应酸能使紫色石蕊溶液变________色,使无色酚酞溶液_______色(2)酸与活泼金属反应(3)酸与金属氧化物反应红不变稀盐酸稀硫酸(4)酸与碱反应(中和反应)(5)酸与某些盐反应二、碱的性质(请对应完成后面练习12~20题)1.物理性质(1)氢氧化钠(2)氢氧化钙俗名烧碱、________、________熟石灰、________,水溶液称________颜色状态_