专题化学实验基础2.实验室利用乙醇脱水制备乙烯的步骤如下;①在蒸馏烧瓶中加人95%的乙醇和浓硫酸(体积比为l:3),再加入少量碎瓷片;②瓶口插上带塞的温度计;③加热并迅速使反应温度上升到170℃;④气体通过稀NaOH溶液进行洗气后,用酸性KMnO4溶液检验乙烯的还原性
据此回答下列问题:(1)步骤①中混合乙醇和浓硫酸时应注意的问题是
(2)在反应液中加入少量碎瓷片的作用是
(3)步骤②中温度计水银球的正确位置是
(4)加热时,使反应液温度迅速升高到170℃的原因是
(5)步骤④中.用稀NaOH溶液洗涤气体,能除去可能伴随乙烯生成的气体是,写出产生此类气体的化学方程式
3.现有Wg的混合气体,其主要成分是CO、H2和少量CO2、水蒸气
请从下图中选用适当的实验装置设计一个实验,以确认上述混合气中含有CO和H2,并计算H2的质量分数
(1)应选用的装置(只要求写出图中的装置序号)__________________________
(2)所选用的装置的连接顺序应是(填各接口的字母,连接胶管省略)
混合气体→_____________________
(3)确认混合气体中含H2的实验现象__________________________,理由是_______________________
(4)实验前分别称装置⑥质量为W1g、装置⑤为M1g、装置②为Z1g
实验结束后再称各装置:装置⑥为W2g、装置⑤M2g、装置②为Z2g
若反应中生成物全被吸收,则Wg混合气中H2的质量分数为_______
实验室用下列装置所示的流程进行气体性质实验
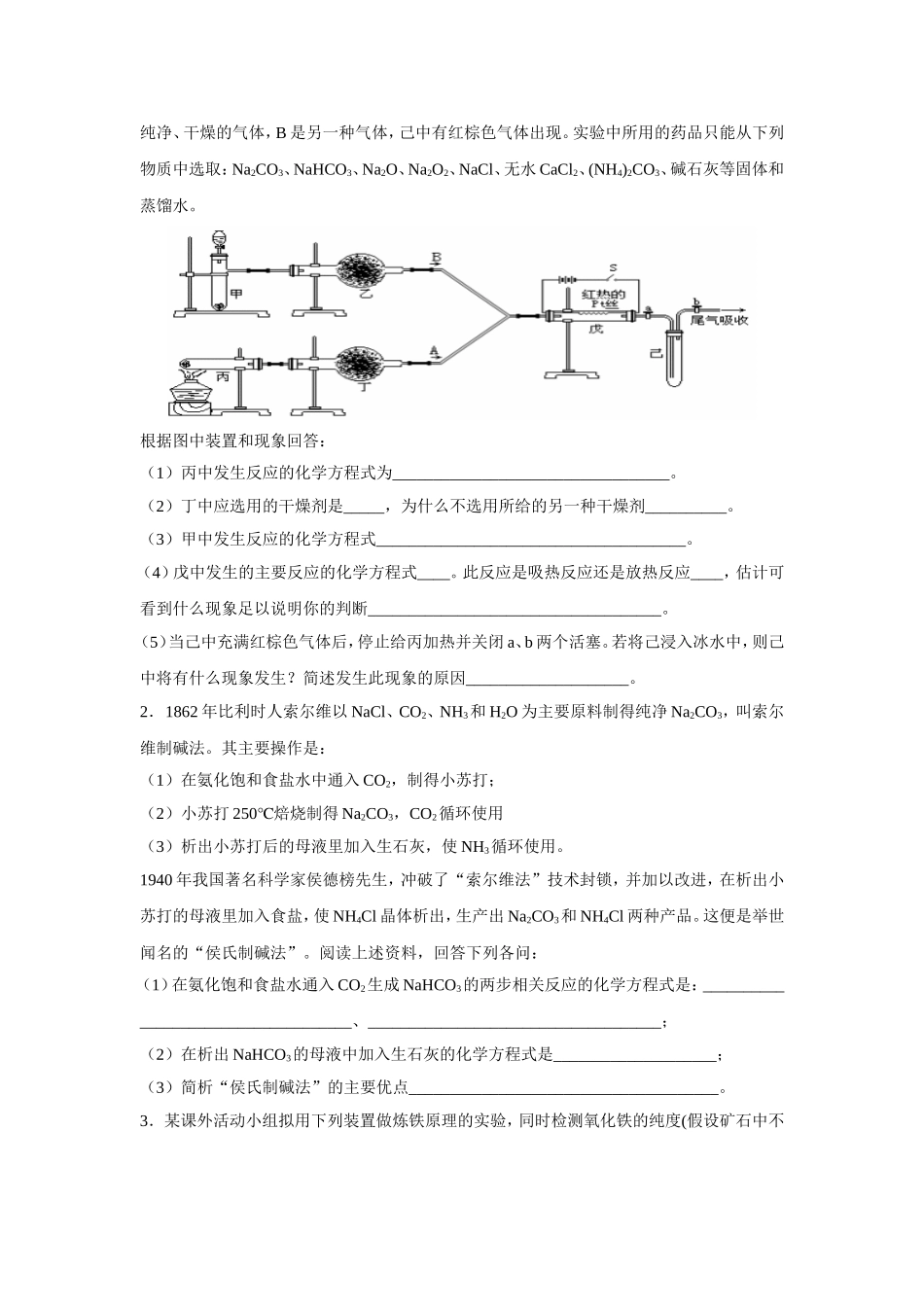
图中用箭头表示气体的流向,A为一种纯净、干燥的气体,B是另一种气体,己中有红棕色气体出现
实验中所用的药品只能从下列物质中选取:Na2CO3、NaHCO3、Na2O、Na2O2、NaCl、无水CaCl2、(NH4)2CO3、碱石灰等固体和蒸