潼关县四知中学陈振华(—)课题31
能知道实验室制取氧气的方法、原理和装置
能理解催化剂及催化作用的概念
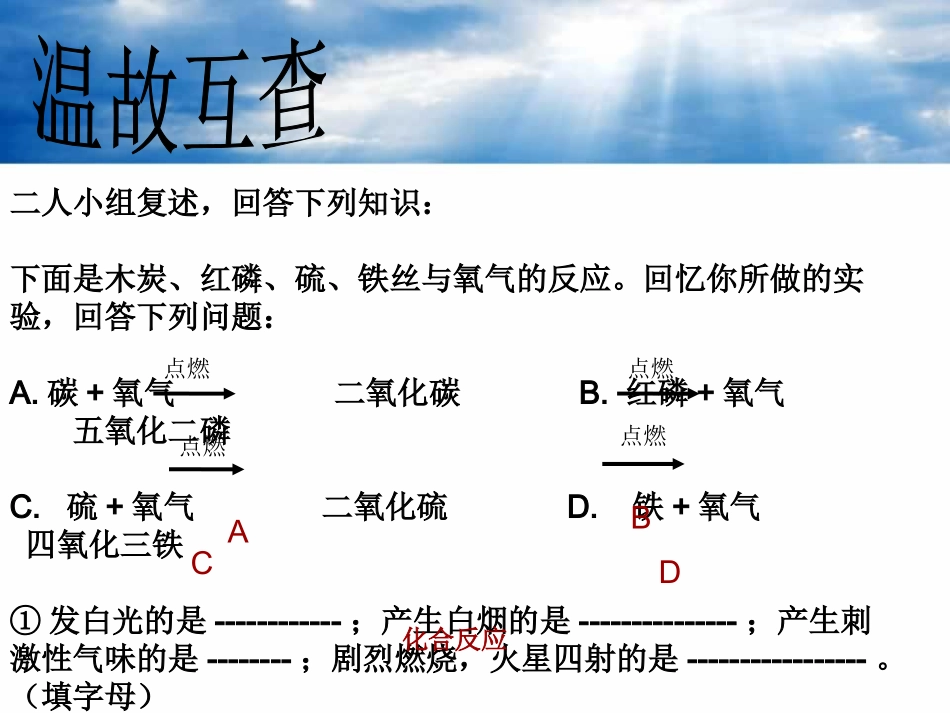
能初步区别化合反应和分解反应【学习目标】二人小组复述,回答下列知识:下面是木炭、红磷、硫、铁丝与氧气的反应
回忆你所做的实验,回答下列问题:A
碳+氧气二氧化碳B
红磷+氧气五氧化二磷C
硫+氧气二氧化硫D
铁+氧气四氧化三铁①发白光的是------------;产生白烟的是---------------;产生刺激性气味的是--------;剧烈燃烧,火星四射的是-----------------
(填字母)②上述反应的基本类型是---------------
点燃点燃点燃点燃ABCD化合反应阅读课本第37页并观察实物,回答下列问题:[问题]实验室制取氧气有哪些方法
⑴实验室制取氧气通常采用分解无色的---------溶液;加热-----------色高锰酸钾固体或白色的-----------固体
⑵分解过氧化氢溶液制取氧气的探究过氧化氢暗紫色氯酸钾探究分解过氧化氢制氧气的反应中二氧化锰的作用•(1)在试管中加入5mL5%的过氧化氢溶液,把带火星的木条伸入试管,观察现象
•⑵向上述试管中,加入少量二氧化锰,把带火星的木条伸入试管
观察发生的现象
•⑶待上述试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,观察现象
待试管中又没有现象发生时,再重复上述操作,观察现象
[实验探究]同学们观察后,小组讨论完成下列表格:实验主要现象原因⑴⑵⑶木条不复燃产生的氧气少木条复燃二氧化锰加快了过氧化氢溶液的分解木条多次复燃二氧化锰是过氧化氢溶液分解的催化剂实验结论•①过氧化氢溶液在常温下--------------(填‘能’或‘不能’)分解,但是分解速率----------,产生的氧气-----------------
•②放二氧化锰粉末后---------