氮的固定氮的固定将空气中将空气中游离的氮游离的氮转变为转变为氮的化合物氮的化合物的方法的方法叫做氮的固定
叫做氮的固定
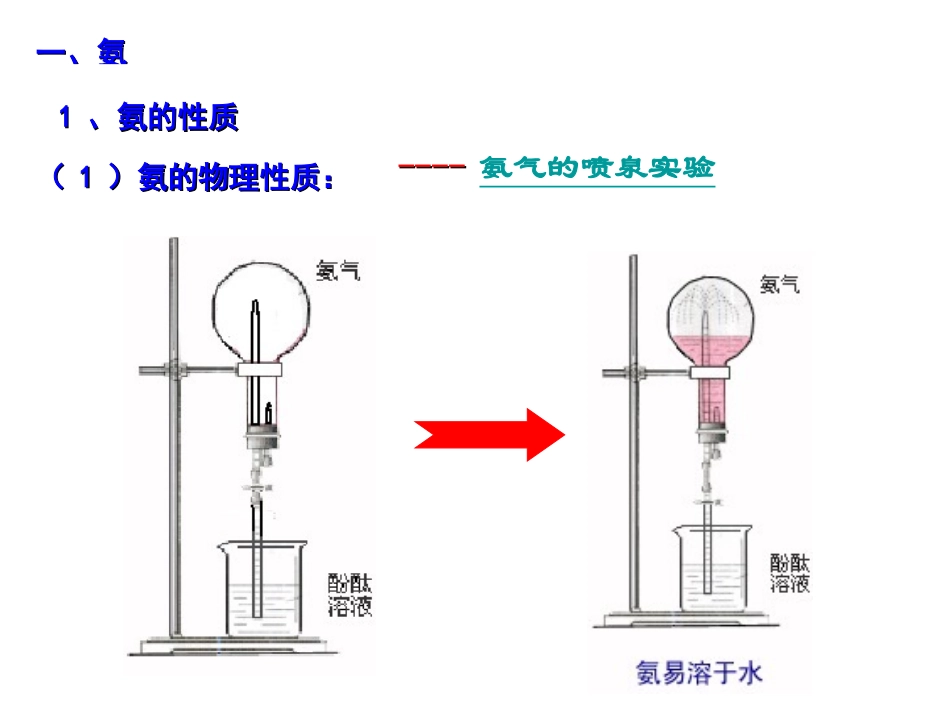
氮氮的的固固定定自然自然固氮固氮人工人工固氮:固氮:合成氨合成氨打雷放电打雷放电条件下固氮条件下固氮豆科植物豆科植物根瘤菌固氮根瘤菌固氮NN22+3H+3H222NH2NH33高温、高压高温、高压催化剂催化剂--------氨气的喷泉实验一、氨一、氨11、氨的性质、氨的性质((11)氨的物理性质:)氨的物理性质:实验现象:a
烧杯内的水由玻璃管进入烧瓶内形成喷泉;b
烧瓶内溶液呈红色
((22)溶液为什么变为红色
)溶液为什么变为红色
((11)氨为什么会形成喷泉
)氨为什么会形成喷泉
氨气溶于水溶液显碱性氨气溶于水溶液显碱性氨极易溶于水,使烧瓶内外形成较大的压差;氨极易溶于水,使烧瓶内外形成较大的压差;((11)氨的物理性质:)氨的物理性质:无色有刺激性气味的气体无色有刺激性气味的气体ρρ(NH3)∶(NH3)∶ρρ((空空气气)=)=极易溶于水,极易溶于水,17∶2917∶29密度比空气小,密度比空气小,体积比体积比1∶7001∶700易液化(可做制冷剂)易液化(可做制冷剂)氨气的水溶液呈碱性氨气的水溶液呈碱性颜色状态:密度:水溶性:①①氨与水反应:氨与水反应:(一水合氨)(一水合氨)aa、氨水显、氨水显弱碱性弱碱性
能使酚酞溶液变红或使红
能使酚酞溶液变红或使红色石蕊试纸变蓝
色石蕊试纸变蓝
NHNH33+H+H22OONHNH33·H·H22OO分子:分子:NHNH33、、HH22OO、、NHNH33·H·H22OO离子:离子:NHNH44++、、OHOH--、、(H(H++))bb、氨水的成分、氨水的成分NHNH44+++OH+OH--((22)氨的化学性质:)氨的化学性质:CC、、NHNH33·H·H22OO的的不稳定性不稳定性NHNH33·H