1⑴不用浓盐酸原因是⑵不用稀硫酸的原因是注意事项装置,药品和实验步骤都要常见气体的制取与净化☆☆考点一常见气体的制取、几种常见气体制取的比较⑴试管口应略倾斜⑵导管应刚露出胶塞⑶用高锰酸钾制氧试管口处应—⑷铁夹应夹在试管中上部
⑸排水法收集时,当时才收集
⑹结束时应先再⑺分液漏斗的优点
⑶不用碳酸钠,碳酸钙原因是⑷长颈漏斗末端应⑸排空气法收集气体时应把导管伸到一、气体制取的装置1、气体的发生装置:气体发生装置的选择原则:根据要制取的气体所需的反应条件(如常温、加热、加催化剂等)、反应物(药品)的状态等来确定
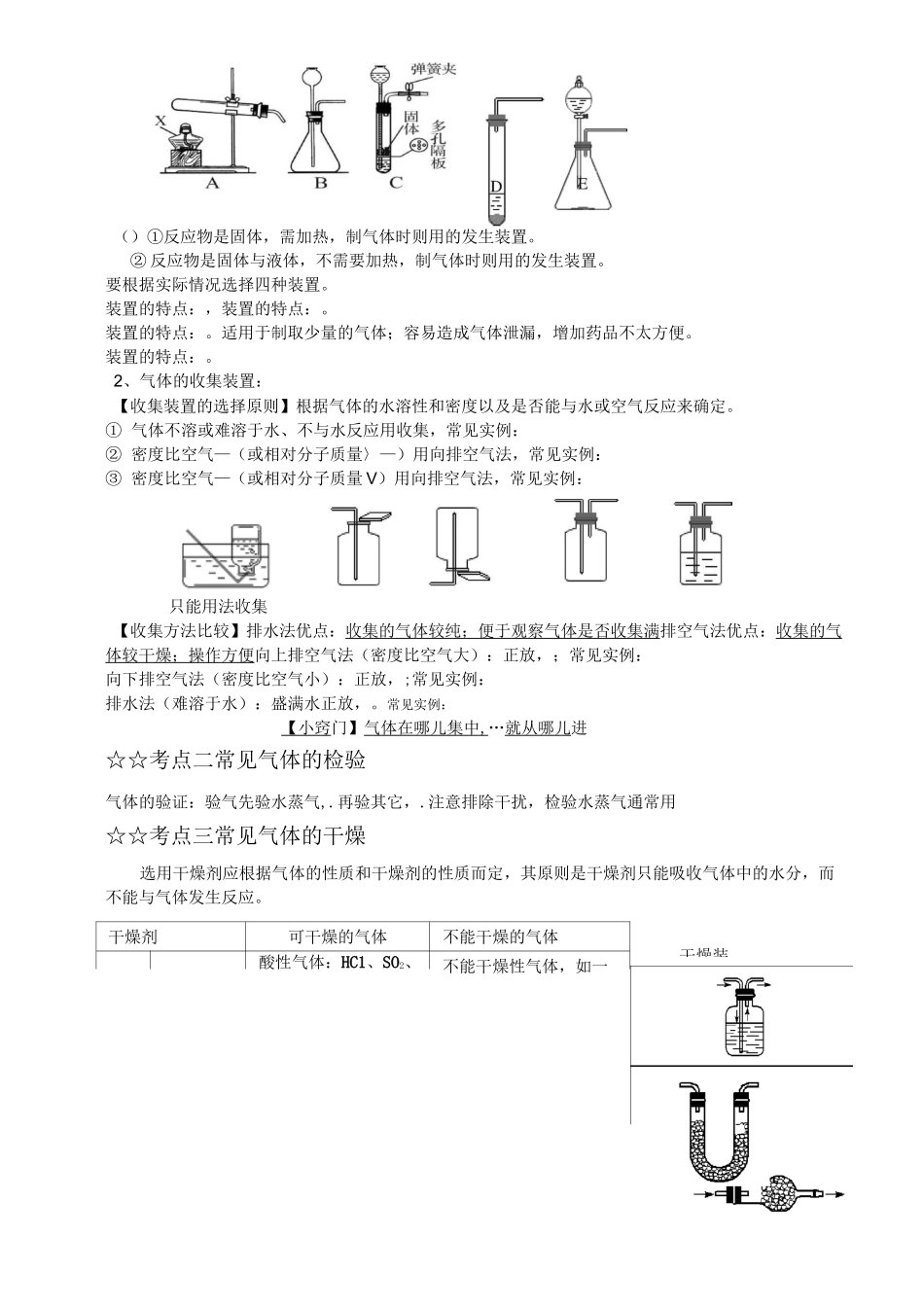
药品选择原则(1)原料廉价易得⑵速率快慢适中⑶生成气体尽量氧气二氧化碳氢气纯净反应原理生成气体尽量纯反应装置反应物状态和反应条件一般可用以下套装置制取收集装置气体溶解性和密度验满方法检验方法根据气体的性质选择点燃气体,火焰为淡蓝色,用干燥的烧杯罩在火焰上方,烧杯内壁有水珠点燃的木条放在试管口,有轻微爆鸣声,说明已满实验操作步骤先后顺序不能颠倒⑴⑵装药品⑶固定试管⑷点燃酒精灯⑸收集⑹⑴⑵加入石灰石⑶加入稀盐酸⑷收集干燥剂可干燥的气体不能干燥的气体酸性气体:HC1、SO2、不能干燥性气体,如一干燥装()①反应物是固体,需加热,制气体时则用的发生装置
②反应物是固体与液体,不需要加热,制气体时则用的发生装置
要根据实际情况选择四种装置
装置的特点:,装置的特点:
装置的特点:
适用于制取少量的气体;容易造成气体泄漏,增加药品不太方便
装置的特点:
2、气体的收集装置:【收集装置的选择原则】根据气体的水溶性和密度以及是否能与水或空气反应来确定
①气体不溶或难溶于水、不与水反应用收集,常见实例:②密度比空气—(或相对分子质量〉—)用向排空气法,常见实例:③密度比空气—(或相对分子质量V)用向排空气法,常见实例:只能用法收集【收集方法比较】排水法优点:收集的气体较纯;便于观察气体是否