课题1原电池一、原电池工作原理1.原理图示2.原电池的判断方法(1)先分析有无外接电源,有外接电源的为电解池,无外接电源的可能为原电池,然后依据原电池的形成条件分析判断,主要是“四看”:看电极——两极为导体且存在活泼性差异(燃料电池的电极一般为惰性电极);看溶液——两极插入溶液中;看回路——形成闭合回路或两极直接接触;看本质——有无氧化还原反应发生
(2)多池相连,但无外接电源时,两极活泼性差异最大的一池为原电池,其他各池可看作电解池
【例1】在盛有稀硫酸的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是()A.正极附近的SO浓度逐渐增大B.电子通过导线由铜片流向锌片C.正极有O2逸出D.铜片上有H2逸出解析:本题符合铜锌原电池的形成条件,原电池工作时,电子由负极(锌)经外电路(导线)流向正极(铜)
负极锌片:Zn-2e-===Zn2+;正极铜片:2H++2e-===H2↑;总反应为:Zn+2H+===Zn2++H2↑
原电池中没有产生O2
SO向负极移动
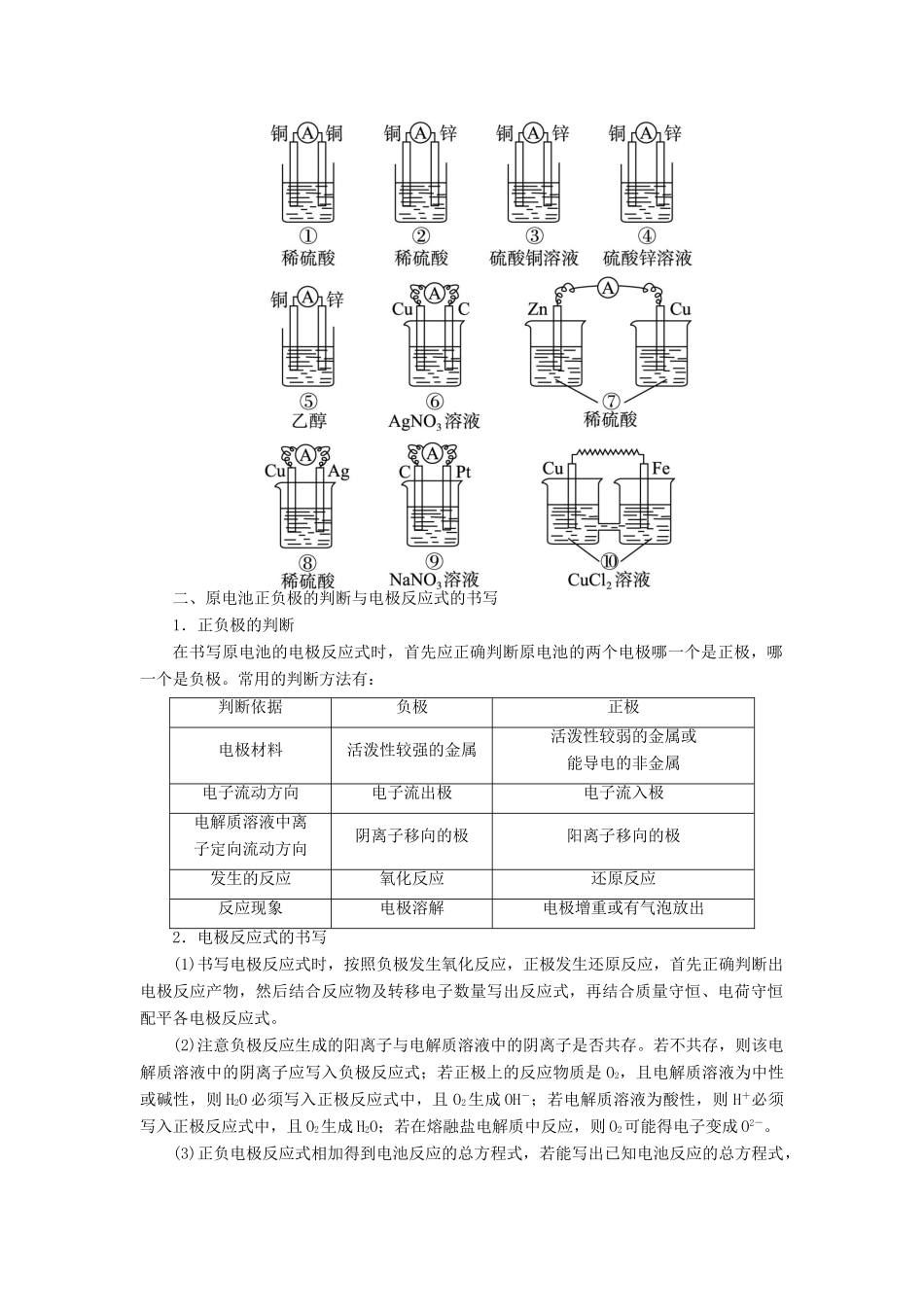
答案:D1-1下列装置中明显有电流产生的是()二、原电池正负极的判断与电极反应式的书写1.正负极的判断在书写原电池的电极反应式时,首先应正确判断原电池的两个电极哪一个是正极,哪一个是负极
常用的判断方法有:判断依据负极正极电极材料活泼性较强的金属活泼性较弱的金属或能导电的非金属电子流动方向电子流出极电子流入极电解质溶液中离子定向流动方向阴离子移向的极阳离子移向的极发生的反应氧化反应还原反应反应现象电极溶解电极增重或有气泡放出2.电极反应式的书写(1)书写电极反应式时,按照负极发生氧化反应,正极发生还原反应,首先正确判断出电极反应产物,然后结合反应物及转移电子数量写出反应式,再结合质量守恒、电荷守恒配平各电极反应式
(2)注意负极反应生成的阳离子与电解质溶液中的阴离子是否共存
若不共存,则该电解质溶液中的阴离子应写入负极