第2章化学能与热能●知识要点一、化学键与化学反应中能量变化的关系1.化学反应的实质化学反应的实质是原子(或原子团)的重新组合,即反应物中化学键的断裂和生成物中化学键的形成
2.化学反应中能量变化的原因(微观角度)(1)物质中的原子(或原子团)之间是通过化学键相结合的
(2)当物质发生化学反应时,断开反应物中的化学键要吸收能量,而形成生成物中的化学键要放出能量
(3)化学键的断裂与形成是化学反应中能量变化的主要原因
例如:断开H-H键要吸收能量436k形成H-H键要放出能量436kJ
1molCH4中含有4molC-H键,断开1molC-H键要吸收415kJ热量,断开1molCH4中的C-H键需要吸收4×415=1660kJ
H2+Cl2===2HCl(5)化学反应中能量变化的计算以H2+Cl2===2HCl为例:断裂化学键吸收的能量形成化学键放出的能量H2Cl2HCl1mol化学键436kJ243kJ431kJ共吸收436kJ+243kJ=679kJ共放出862kJ679kJ-862kJ=-183kJ,即反应放出183kJ热量计算公式为ΔQ=Q(吸)-Q(放)特别提示:公式中Q(吸)表示反应物断裂所有化学键吸收的能量和,Q(放)表示形成生成物所有化学键放出的能量和
3.化学反应中能量变化的决定因素(宏观角度)能量守恒定律1(4)键能:拆开1mol某键所需的能量叫键能
单位:kJ/mol
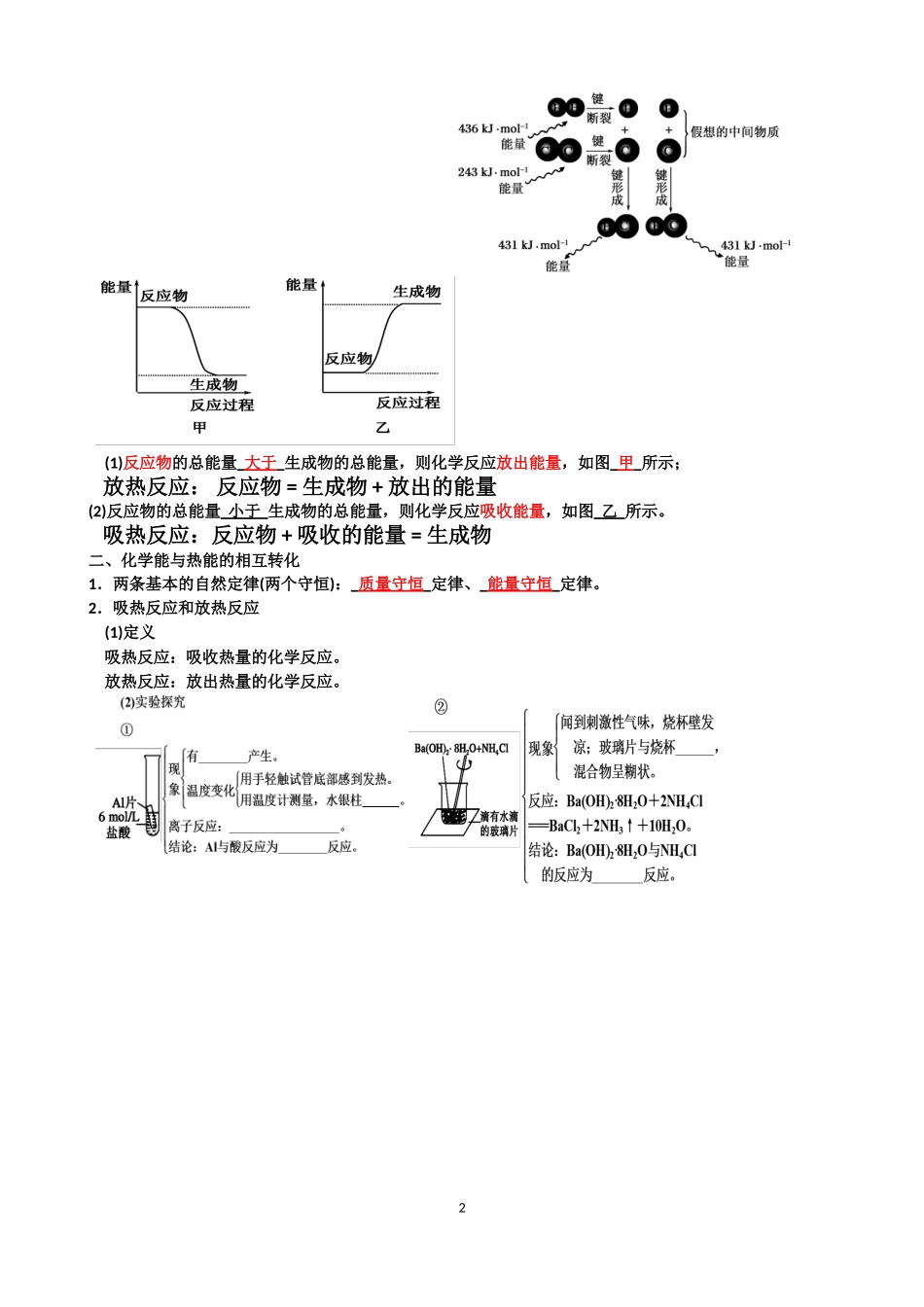
取决于所有断键吸收的总能量与所有形成新键放出的总能量的相对大小(6)小结:一个化学反应是否为放热还是吸热取决于键能(微观角度)放热反应:反应物总键能生成物总键能吸热反应:(1)反应物的总能量大于生成物的总能量,则化学反应放出能量,如图甲所示;放热反应:反应物=生成物+放出的能量(2)反应物的总能量小于生成物的总能量,则化学反应吸收能量,如图乙所示
吸热反应:反应物+吸收的能量=生成物二、化学