第二节气体摩尔体积新课指南1
在了解气体的体积与温度和压强有密切关系的基础上,理解气体摩尔体积的概念
掌握有关气体摩尔体积的计算
通过气体摩尔体积和有关计算的学习,培养分析、推理、归纳、总结的能力
本节重点:气体摩尔体积的概念和有关气体摩尔体积的计算
本节难点:气体摩尔体积的概念及其推论的应用
教材解读精华要义1
物质的体积、密度和质量之间的关系物质的质量跟它的体积的比叫做这种物质的密度,即物质在单位体积中所含的质量,叫做该物质的密度
计算1mol不同固态物质和液态物质的体积(见下表)物质1mol该物质的质量密度1mol的物质所具有的体积Fe56g7
8g/cm3(20℃)7
2cm3Al27g2
7g/cm3(20℃)10cm3Pb207g11
3g/cm3(20℃)18
3cm3H2O18g1g/cm3(4℃)18cm3H2SO498g1
83g/cm3(20℃)53
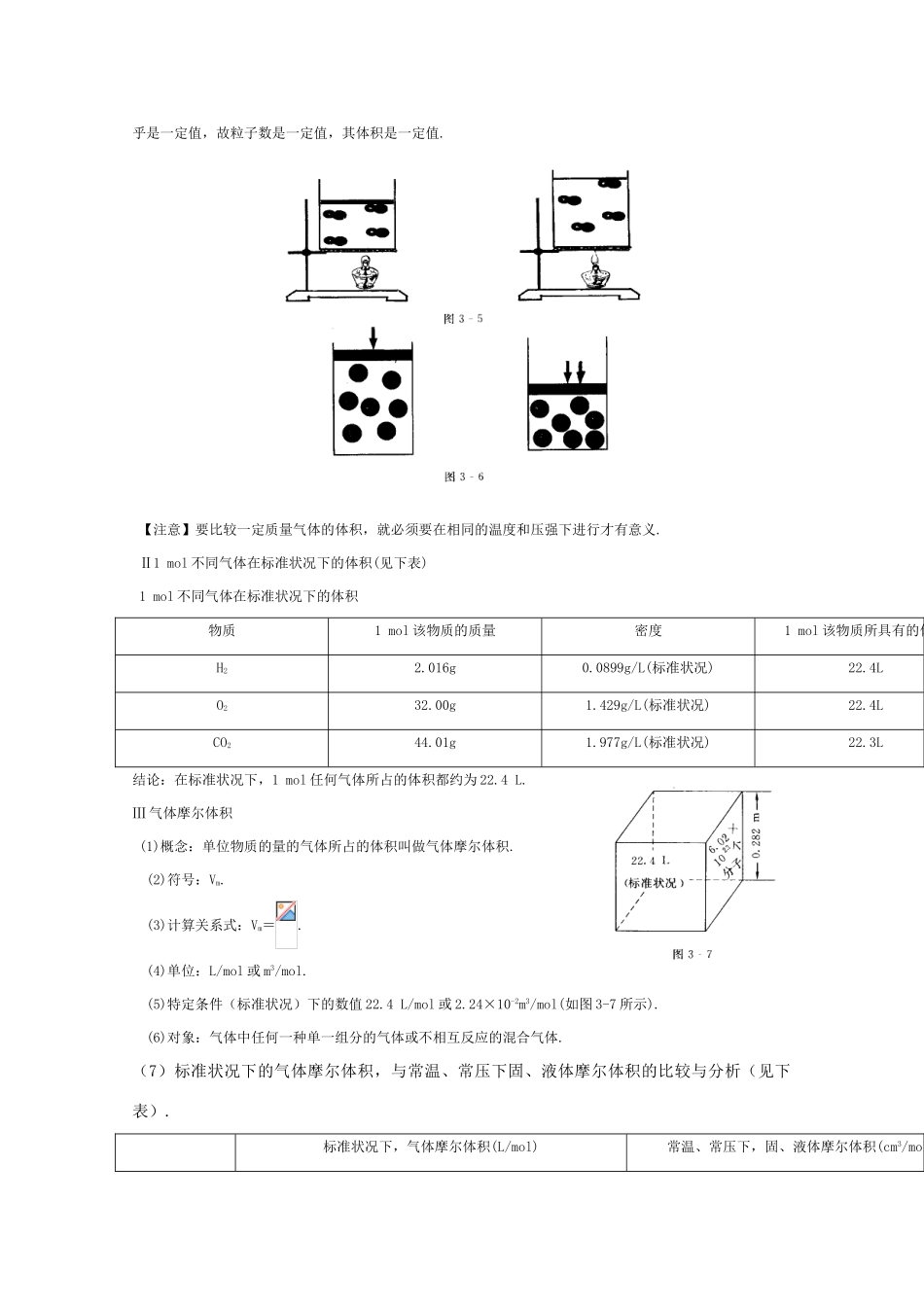
归纳1mol不同固态物质和液态物质体积的特点并分析其形成差异的主要原因Ⅰ对于固态物质和液态物质来说,1mol不同物质的体积一般是不同的(如图3-2所示)
Ⅱ决定物质的体积大小有三大因素
(1)物质粒子数的多少
(2)物质粒子之间距离的大小
(3)物质粒子的大小(直径为d)
Ⅲ形成差异的主要原因
构成液态、固态物质的粒子间的距离是很小的,在粒子数相同的条件下,固态、液态物质的体积主要决定于原子、分子或离子本身的大小;由于构成不同,物质的原子、分子或离子的大小也是不同的,所以它们1mol的体积也就有所不同(如图3-3所示)
知识详解知识点1气体摩尔体积(重点、难点)Ⅰ决定气体体积大小的主要因素(1)决定气体所含有的分子数(或气体的物质的量)
在一定温度,一定压强下,气体中所含的分子数目(或物质的量)越多,气体的体积就越大
(2)分子的直径和分子之间的距离
一般来说,气体分子的直径约为0