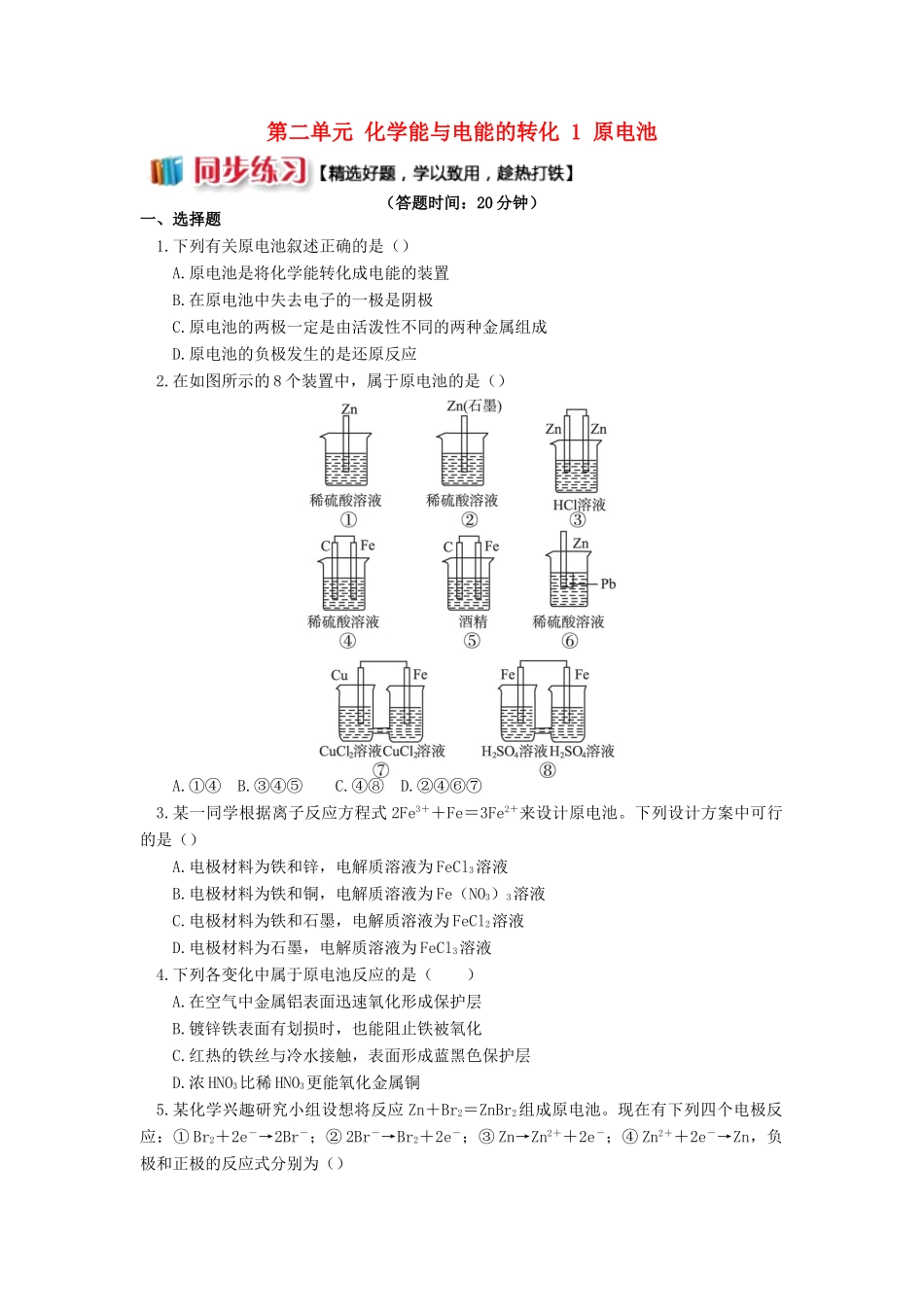
第二单元化学能与电能的转化1原电池(答题时间:20分钟)一、选择题1.下列有关原电池叙述正确的是()A.原电池是将化学能转化成电能的装置B.在原电池中失去电子的一极是阴极C.原电池的两极一定是由活泼性不同的两种金属组成D.原电池的负极发生的是还原反应2.在如图所示的8个装置中,属于原电池的是()A.①④B.③④⑤C.④⑧D.②④⑥⑦3.某一同学根据离子反应方程式2Fe3++Fe=3Fe2+来设计原电池。下列设计方案中可行的是()A.电极材料为铁和锌,电解质溶液为FeCl3溶液B.电极材料为铁和铜,电解质溶液为Fe(NO3)3溶液C.电极材料为铁和石墨,电解质溶液为FeCl2溶液D.电极材料为石墨,电解质溶液为FeCl3溶液4.下列各变化中属于原电池反应的是()A.在空气中金属铝表面迅速氧化形成保护层B.镀锌铁表面有划损时,也能阻止铁被氧化C.红热的铁丝与冷水接触,表面形成蓝黑色保护层D.浓HNO3比稀HNO3更能氧化金属铜5.某化学兴趣研究小组设想将反应Zn+Br2=ZnBr2组成原电池。现在有下列四个电极反应:①Br2+2e-→2Br-;②2Br-→Br2+2e-;③Zn→Zn2++2e-;④Zn2++2e-→Zn,负极和正极的反应式分别为()A.②③B.②①C.③①D.④①6.把a、b、c、d四块金属浸入稀硫酸中,用导线两两连接组成多个原电池,若a、b相连,a为负极;c、d相连,d上有气泡逸出;a、c相连,a极减轻;b、d相连,b为正极。则四种金属的活泼性顺序为()A.a>b>c>dB.a>c>b>dC.a>c>d>bD.b>d>c>a7.表明金属甲比金属乙活泼性强的是()A.在氧化还原反应中,甲失电子比乙多B.同价态的阳离子,甲比乙氧化性强C.甲能与盐酸反应放出氢气而乙不能D.将甲、乙组成原电池时,甲为正极二、填空题8.熔盐电池具有较高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气为阴极助燃气,制得在650℃下工作的燃料电池,完成有关电池反应式。阳极反应式:2CO+2CO32-=4CO2+4e-,阴极反应式:。电池总反应式:。9.利用反应Cu+2FeCl3=CuCl2+2FeCl2组成一个化学电池。(1)指出正极为________,电极反应式为__________________________________;负极为____________,电极反应式为____________________________。(2)若电池内溶液为100mL0.5mol/L的FeCl3溶液;当溶液中FeCl3全部被还原成FeCl2时,溶液中CuCl2的物质的量浓度是________,导线上通过的电子是________mol。10.⑴今有反应2H2+O22H2O,设计成燃料电池,则负极通的应是,正极通的应是电极反应式为:、。⑵如把KOH改为稀H2SO4作电解质,则电极反应式为:、。⑴和⑵的电解液不同,反应进行后,其溶液的pH值变化为、。⑶如把H2改为甲烷,KOH作电解质,则负极反应式为:。一、选择题1.A解析:原电池是将化学能转化为电能的装置,失去电子的一极是负极,发生氧化反应。原电池的两极可以是两种活泼性不同的金属,也可以为金属与非金属。2.D解析:根据原电池中有两个电极可以排除掉①;而且两电极活泼性不同,排除③、⑧;注意②⑥都含有两种活泼性不同的金属或非金属,即含有两个电极;必须存在电解质溶液,可排除⑤;②④⑥⑦都满足形成原电池的条件。3.B解析:氧化还原反应中的还原剂作原电池的负极,氧化剂(Fe3+)存在于电解质溶液中,故符合题意的选项为B。4.B解析:A、C、D项为化学腐蚀;B项Zn作负极,Fe作正极,在潮湿环境中构成原电池,Zn被腐蚀,Fe受到保护;C项3Fe+4H2O(g)Fe3O4+4H2;D项浓硝酸的氧化性强于稀硝酸,所以更易氧化铜,答案选B。5.C解析:依据原电池的原理可知,负极是失电子的一极,且为电池总反应式中的反应物,故应为③Zn→Zn2++2e-;正极是得电子的一极,且也为电池总反应式中的反应物,故应为①Br2+2e-→2Br-。6.C解析:依据金属的活泼性相对强弱的判断及原电池正、负极的判断可知:a、b相连,a为负极,则a>b;c、d相连,d上有气泡逸出,则c为负极,即c>d;a、c相连,a极减轻,则a为负极,即a>c;b、d相连,b为正极,则d>b。7.C解析:金属甲比金属乙活泼性强,得失电子能力的强弱,与得失电子数目多少无关;而同价态的阳离子,说明乙比甲氧化性强;一般来说...