1常见的金属材料第2课时炼铁的原理炼铁的原理1.一氧化碳还原氧化铁的实验(1)实验装置:(如图所示)(2)实验步骤:实验开始先通入一氧化碳后加热,实验完毕先停止加热,后停止通入一氧化碳
快乐记忆:“一通、二点、三灭、四停、五处理”:“一通”先通一氧化碳,“二点”后点燃酒精灯进行加热;“三灭”实验完毕后,先熄灭酒精喷灯,“四停”等到室温时再停止通一氧化碳;“五处理”处理尾气,防止CO污染环境
(3)实验现象:红色的氧化铁粉末变为黑色,澄清的石灰水变浑浊
(4)反应的化学方程式(炼铁原理):3CO+Fe2O3=====2Fe+3CO2
2.工业炼铁(1)原料:铁矿石、焦炭、石灰石、空气
(2)主要设备:高炉
工业炼铁与实验室“炼铁”的比较炼铁的原理是在高温条件下,用还原剂从铁的氧化物中将铁还原出来
工业炼铁与实验室“炼铁”的主要区别在于:①还原剂不同
工业炼铁的原料有铁矿石、焦炭、石灰石和空气,利用焦炭和空气发生一系列化学反应,得到CO,同时放出大量的热,为反应提供高温条件,而实验室“炼铁”采用直接通入还原剂CO气体的方法
工业炼铁使用高炉,可实现连续投料、连续生产,而实验室“炼铁”使用硬质玻璃管,用酒精喷灯来实现“高温”条件
工业炼铁的产物是含碳量较高的生铁,实验室“炼铁”能得到较纯净的铁
【例题】某校化学小组的同学为了研究炼铁的原理,用一氧化碳与氧化铁反应,按图1进行实验
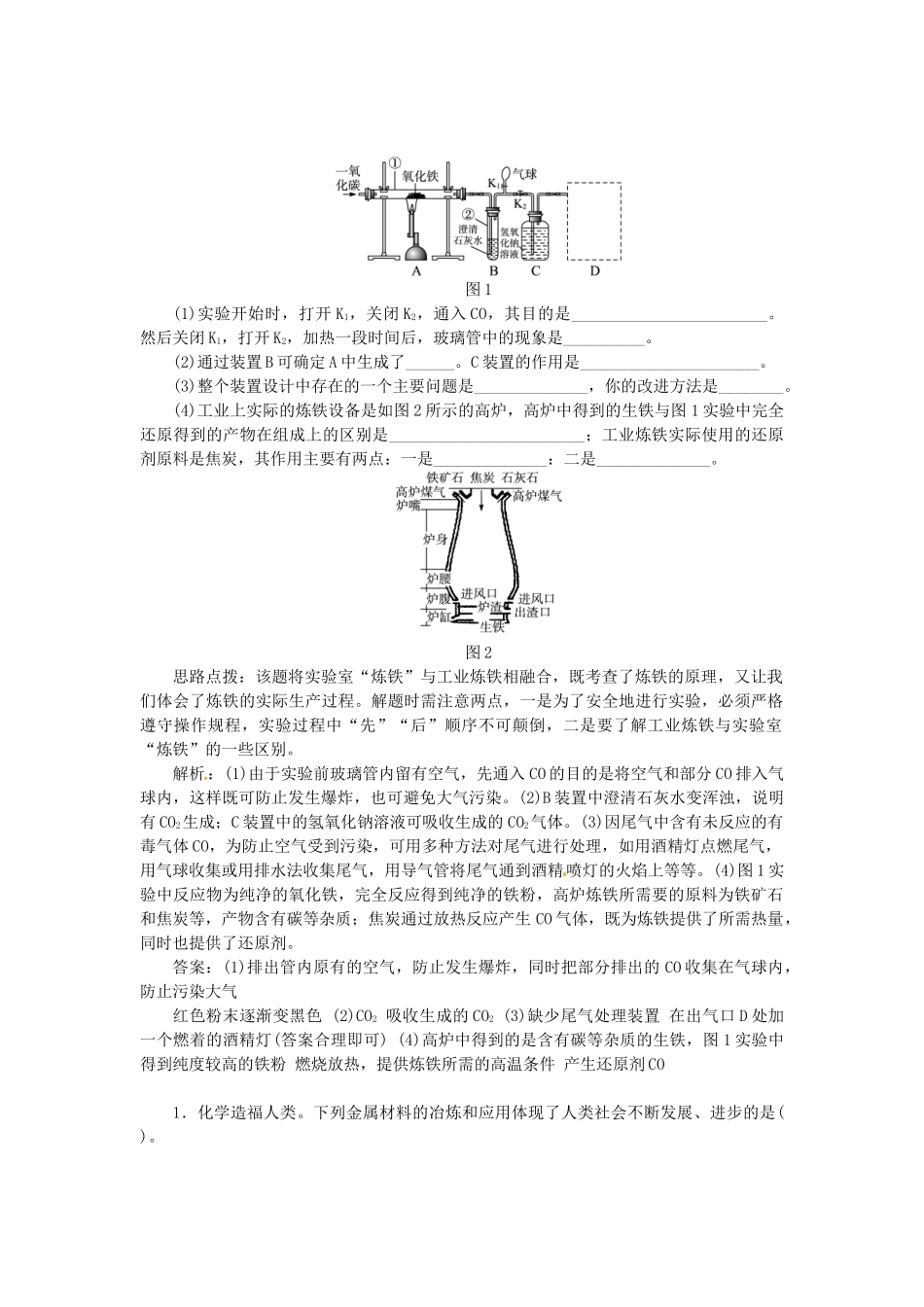
图1(1)实验开始时,打开K1,关闭K2,通入CO,其目的是________________________
然后关闭K1,打开K2,加热一段时间后,玻璃管中的现象是__________
(2)通过装置B可确定A中生成了______
C装置的作用是______________________
(3)整个装置设计中存在的一个主要问题是______________,你的改进方法是_