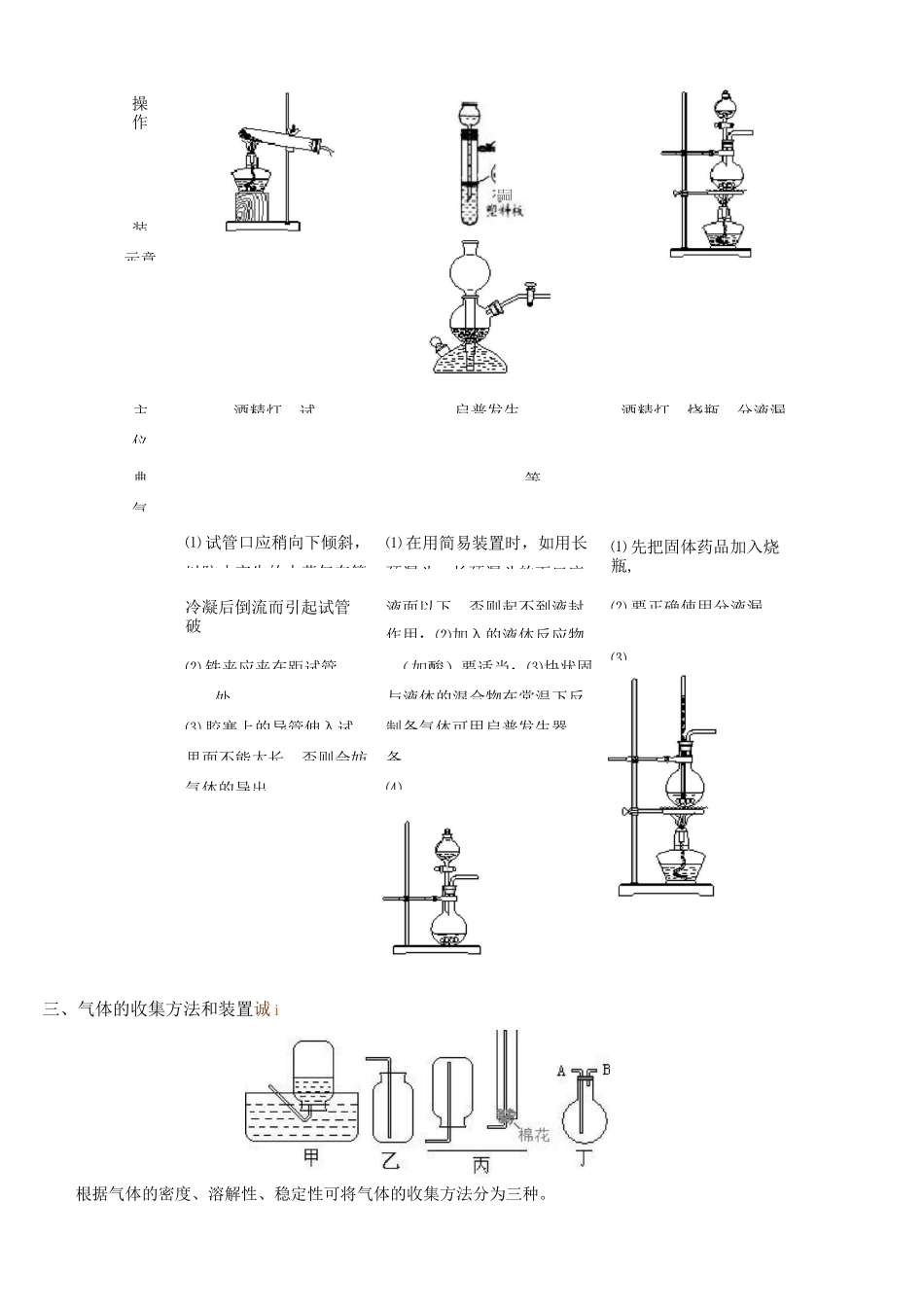
常见气体的制备与收集整理:华侨大学校草级学长【内容讲解】诫i一、几种气体制备的反应原理閉气悴反应原理(化学方程式)氧气2KC1O3'2KC1+3O212KM11O4K2MnO4+MnO2+O21MnO^.2H2O22H2O+0界氨气2NH4Cl+Ca(OH)2」一CaCl2+2NH31+2H2O氢气Zn+H2SO4=ZnSO4+H21co2CaCO3+2HCl=CaCl2+CO21+H2ONa2SO3+H2SO4(;浓)=N电ES+HzO+EChtNO2CU+4HNO3(浓)=CU(N6)2+2N6匸+2母0C2H2CaC2+2H2O一Ca(OH)2+C2H21孰气MnO2+4HCl(浓)=乂MnCh+Cht+2H2ONO3CU+8HNO3(稀)f+4H2OC2H4C2H5OH骋翳①站+际二气体发生装置的类型诫i.设计原则:诫i根据反应原理、反应物状态和反应所需条件等因素来选择反应装置。.装置基本类型:诫i装置类型固体反应物(加热)固液反应物(不加热)固液反应物(加热)装示意主仪典气操作酒精灯、试⑴试管口应稍向下倾斜,以防止产生的水蒸气在管冷凝后倒流而引起试管破⑵铁夹应夹在距试管处⑶胶塞上的导管伸入试里面不能太长,否则会妨气体的导出。启普发生等。⑴在用简易装置时,如用长颈漏斗,长颈漏斗的下口应液面以下,否则起不到液封作用;⑵加入的液体反应物(如酸)要适当;⑶块状固与液体的混合物在常温下反制备气体可用启普发生器备。酒精灯、烧瓶、分液漏⑴先把固体药品加入烧瓶,⑵要正确使用分液漏三、气体的收集方法和装置诚i根据气体的密度、溶解性、稳定性可将气体的收集方法分为三种。嗣⑷⑶、收集方法:诫.i、排水集气法凡难溶于水或微溶于水,又不与水反应的气体都可用排水法收集,如图甲。、排空气法一种是向上排空气法,凡是气体的相对分子质量大于空气的平均相对分子质量的可用此法,如图乙;若气体的相对分子质量小于空气的平均相对分子质量,则用向下排空气法,如图丙。、收集装置:诫i图甲可收集、、、饱和溶液、、饱和溶液、等。图乙可收集、、、等。图丙可收集、、等。图丁从进气相当于图乙,从进气相当于图丙。四、气体的干燥净化装置―、气体干燥净化装置眩气体的净化、干燥装置一般常用的有洗气瓶、干燥管、形管和双通加热管几种。液态干燥剂固态干燥剂固体,加热装置甲乙U丙e丁常见干燥剂浓硫酸酸性、强氧化性无水氯化钙中性碱石灰碱性除杂试剂、、等可干燥的气体、、、、、、、、、、、、、、、、、、、可除去、、、不可干燥的气体、、、、、等洗气瓶中一般装入液体除杂试剂。除杂试剂应通过化学反应将杂质吸收或将杂质气体转化为所制取的气体。常见除杂试剂有:①强碱溶液:如溶液可吸收、、、、等呈酸性的气体。②饱和的酸式盐溶液,可将杂质气体吸收转化,如:饱和溶液能除去中混有的、等强酸性气体。饱和溶液能除去中混有的、等气体。饱和溶液能除去中混有的气体。③浓:利用它的吸水性,可除去、、、、、等气体中混有的水蒸气。但由于浓有强氧化性,不能用来干燥具有强还原性气体,如、、等。④酸性溶液:利用它的强氧化性,可以除去具有还原性的气体,如除去混在气体中的、等。干燥管、形管一般装入固体的干燥剂。常见的固体干燥剂有:①酸性干燥剂,用来干燥酸性气体。如、硅胶等。②碱性干燥剂,用来干燥碱性气体。如、碱石灰、固体等。③中性干燥剂,既能干燥碱性气体又能干燥酸性气体。如但不能干燥,因易形成•氨,其中和必须排放到室外。利用气体的不溶于某些液体的性质如难溶于水,难溶于饱和食盐水可用排液法粗略测量气体的体积。其合物。双通加热管一般装入固体除杂剂,除杂试剂和混合气体中的某一组分反应。例如:和混合气体中反应而将除去。另外还常用固体的无水装入干燥管中,通过颜色变化检验水蒸气的存在但不能用作干燥剂,因吸水率低。用固体也可将、气转化为。、尾气处理装置应尾气处理与净化、干燥的原理和装置是一样的。图甲装置中若装可吸收、、、等酸性气体。若装可吸收、、等。图乙和图丙装置中若装碱石灰可吸收、、、等酸性气体,同时他们还是一个双吸收装置,应用于制取易潮解的物质,如,制无水时,正好可吸收多余的,反应结束后冷却过程中又可吸收回流的空气以防止潮解。尾气处理还可以用下列装置:甲乙甲装置吸收极易溶于水的气体如、等。乙装置吸收溶解度较小的气体如等。丙装置除去可燃的有毒气体如等。无需要吸...