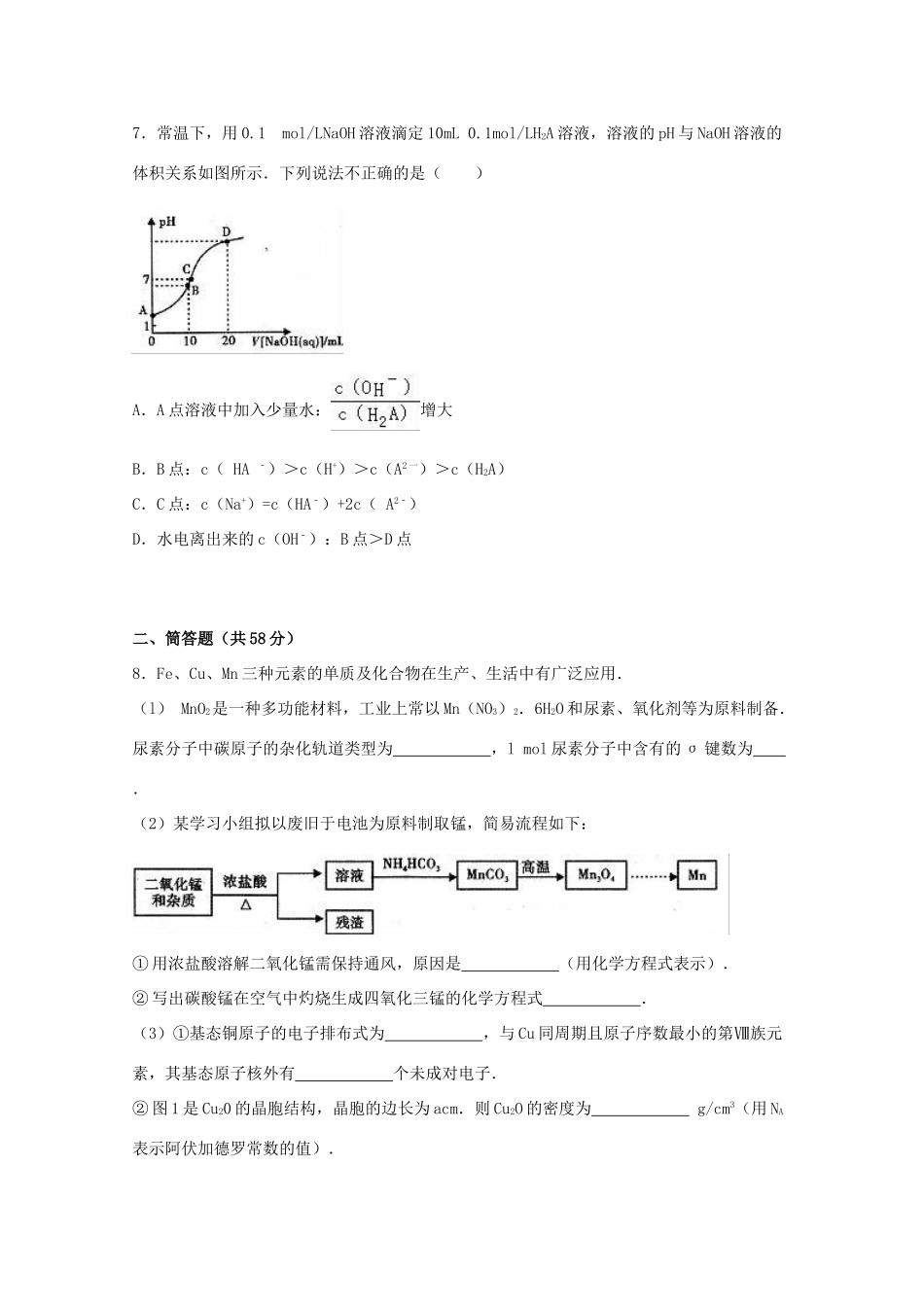
2016年四川省内江市高考化学四模试卷一、选择题(本大题包括7小题,每小题6分,共42分o在每小题给出的四个选项中,只有一个选项符合题目要求).1.化学与社会、生产、生活密切相关.下列说法正确的是()A.为延长食品保质期,可向其中大量添加苯甲酸钠等防腐剂B.催化转化机动车尾气为无害气体,能消除酸雨和雾霾的发生C.PM2.5是指空气中氮氧化物和硫氧化物含量之和D.“地沟油”可以制成肥皂,从而提高资源的利用率2.下列有关NaHS03溶液的叙述正确的是()A.该溶液中,K+、Ca2+、Cl2、Br﹣可以大量共存B.与足量Ca(OH)2溶液反应的离子方程式:Ca2++OH﹣+HS03═CaS03↓+H20C.与FeCI3溶液反应的离子方程式:SO32﹣+2Fe3++H20═SO42﹣+2Fe2++2H+D.能使含I2的淀粉溶液蓝色褪去,说明NaHSO3溶液具有漂白性3.设NA为阿伏加德罗常数的值,下列说法正确的是()A.标准状况下,22.4LHF中含HF分子数目为NAB.60g石英晶体中含有的Si﹣O键数目为2NAC.标准状况下,11.2LCl2通人足量的石灰乳中制备漂白粉,转移的电子数为0.5NAD.lL0.1mol/L的NaHCO3溶液中HCO3﹣和CO32﹣离子数之和为0.1NA4.如图是邵分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是()A.31d和33d属于同种核素B.第一电离能d>e,电负性d<eC.气态氢化物的稳定性:a>d>eD.a和b形成的化合物不可能含共价键5.用无机矿物资源生产部分材料,其生产流程如图.下列有关说法不正确的是()A.Al2O3、SiCl4均为共价化合物B.生产过程中均涉及氧化还原反应C.石英可用于制光导纤维,晶体Si常用做半导体材料D.黄铜矿冶炼铜时产生的SO2可用于生产硫酸,FeO可用于冶炼铁6.下列实验中,对应的现象以及解释或结论都正确且两者具有因果关系的是()选项实验现象解释或结论A向足量的浓硝酸中加入铁片,一段时间后加入铜粉有气体生成,溶液呈蓝绿色浓硝酸将Fe氧化为Fe3+,生成NO2,Cu与Fe3+反应生成Cu2+、Fe2+B分别向MgCl2、AlCl3溶液中加入足量氨水均有白色沉淀产生金属性:Mg>AlC表面变黑的银器浸泡到盛有食盐水的铝制容器中,银器与铝接触银器变得光亮如新构成原电池,铝做负极,硫化银得电子被还原成单质银D向MgSO4稀溶液中滴入NaOH溶液至不再有沉淀生成,再滴加CuSO4稀溶液白色沉淀逐渐变为浅蓝色Kap>KapA.AB.BC.CD.D7.常温下,用0.1mol/LNaOH溶液滴定10mL0.1mol/LH2A溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列说法不正确的是()A.A点溶液中加入少量水:增大B.B点:c(HA﹣)>c(H+)>c(A2一)>c(H2A)C.C点:c(Na+)=c(HA﹣)+2c(A2﹣)D.水电离出来的c(OH﹣):B点>D点二、筒答题(共58分)8.Fe、Cu、Mn三种元素的单质及化合物在生产、生活中有广泛应用.(l)MnO2是一种多功能材料,工业上常以Mn(NO3)2.6H2O和尿素、氧化剂等为原料制备.尿素分子中碳原子的杂化轨道类型为,lmol尿素分子中含有的σ键数为.(2)某学习小组拟以废旧于电池为原料制取锰,简易流程如下:①用浓盐酸溶解二氧化锰需保持通风,原因是(用化学方程式表示).②写出碳酸锰在空气中灼烧生成四氧化三锰的化学方程式.(3)①基态铜原子的电子排布式为,与Cu同周期且原子序数最小的第Ⅷ族元素,其基态原子核外有个未成对电子.②图1是Cu20的晶胞结构,晶胞的边长为acm.则Cu2O的密度为g/cm3(用NA表示阿伏加德罗常数的值).(4)①绿矾(FeS04•7H2O)是补血剂的原料,保存不当易变质.请设计实验检验绿矾是否完全变质.②以羰基化合物为载体,提纯某纳米级活性铁粉(含有一些不反应的杂质),反应装置如图2.已知:Fe(s)+5CO(g)⇌Fe(CO)5△H<0,常压下,Fe(CO)s的熔点约为﹣20.3℃,沸点为103.6℃,则Fe(CO)的晶体类型为.请用平衡移动原理解释T1<T2的原因.9.ClO2是一种高效水处理剂,某实验小组用下图所示装置制取并收集Cl02.已知:①ClO2为黄绿色气体,极易溶于水,熔点﹣59C,沸点11℃,具有强氧化性.②ClO2易爆炸,若用“惰性气体”等稀释时,爆炸的可能性大大降低.③装置A中发生反应:H2C2O4+H2SO4+2KC1O3一K2SO4+2CO2T+2ClO2...