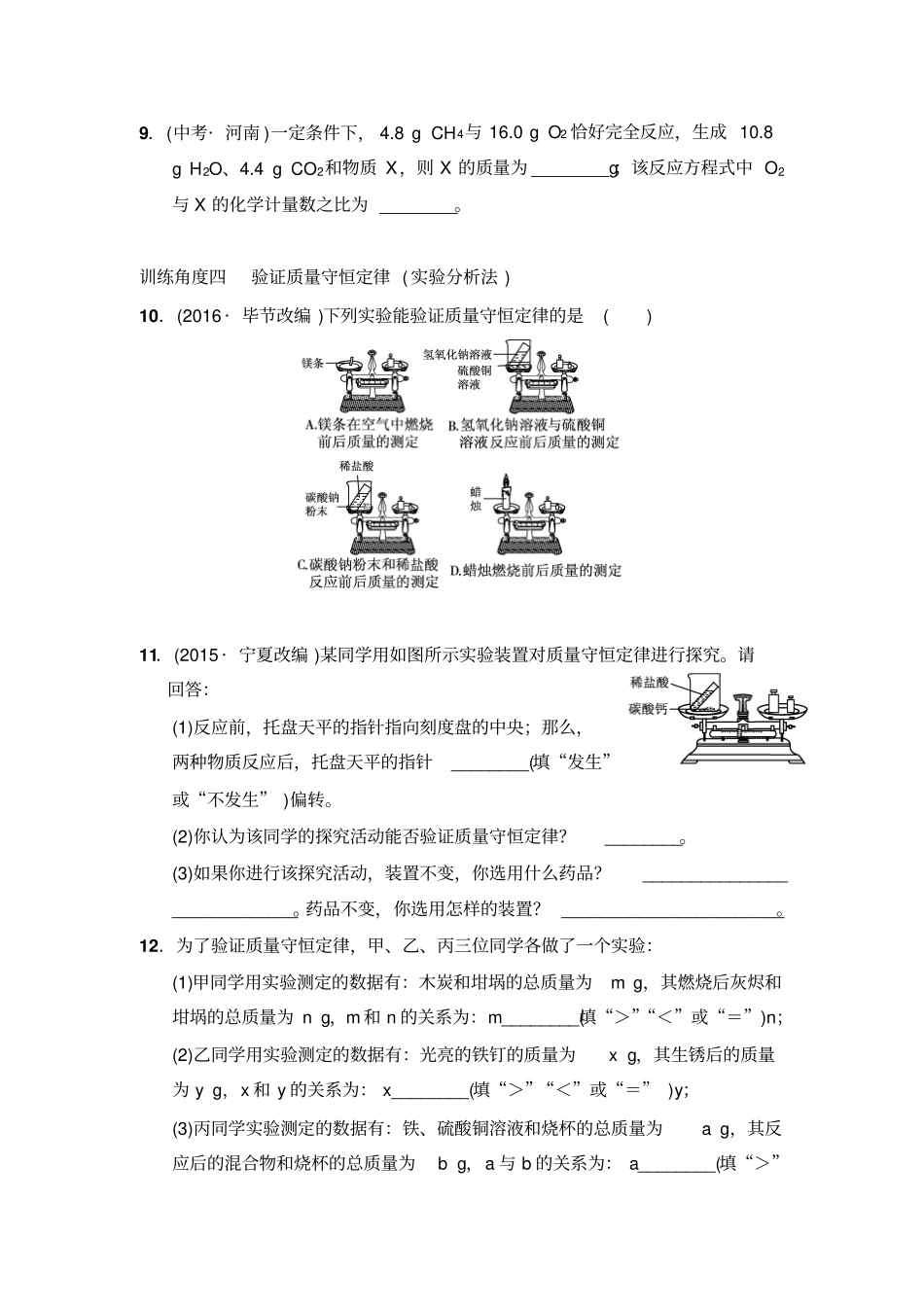
专项训练一:质量守恒定律的应用专项概述质量守恒定律是化学方程式的基础,应记清、理解质量守恒定律,并会用微粒的观点解释质量守恒定律。常涉及的考点有:验证质量守恒定律的探究实验、解释有关现象、利用质量守恒定律判断物质的元素组成或化学式、计算物质的质量等。以上考点也是历年中考的重点。训练角度一质量守恒定律的理解1.下列有关质量守恒定律的理解,正确的是()A.将5g铁和5g铜混合加热后,物质的总质量为10g,遵守质量守恒定律B.化学反应前后分子的总数一定不会发生变化C.5g硫和5g氧气完全反应后,生成物质量为10gD.煤燃烧后质量减轻,不遵守质量守恒定律2.(2015·贵阳)建立基本的化学观念可以让我们更好地理解化学,如形成守恒观念,可以更好地理解质量守恒定律,下列表述正确的是()A.每1个C原子和1个O2分子反应,生成2个CO2分子B.32gS与32gO2完全反应,生成64gSO2C.镁条燃烧后固体质量增加,故质量守恒定律不是普遍规律D.根据:蜡烛+氧气――→点燃二氧化碳+水,则蜡烛中一定含有C、H、O三种元素训练角度二判断物质的组成(守恒法)3.(2016·齐齐哈尔)在催化剂并加热的条件下,氨气和氧气能发生化学反应,其反应的化学方程式为4NH3+5O2=====催化剂△4X+6H2O,则X的化学式是()A.N2B.N2OC.NOD.NO24.(2015·青海)由化学方程式:CxHyOz+5O2=====点燃4CO2+4H2O,可知x、y、z的值分别是()A.4、8、2B.1、2、3C.2、4、1D.4、4、25.(2016·常德)某有机物6.0g在空气中完全燃烧,共得到17.6g二氧化碳和10.8g水,则该化合物的组成元素是()A.一定只含有碳元素B.一定只含有碳、氢两种元素C.一定含有碳、氢、氧三种元素D.一定含有碳、氢元素,可能含有氧元素训练角度三计算物质的质量(守恒法、数据分析法、本质分析法)6.(2016·随州)在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如表所示。根据表中信息判断下列说法正确的是()物质甲乙丙丁反应前的质量/g2302010反应后的质量/gm39516A.该反应是化合反应B.甲是该反应的催化剂C.反应过程中乙、丙变化的质量比为3∶5D.丙可能是单质7.(2015·株洲)已知:X和Y两种物质共80g,在一定条件下恰好完全反应,生成Z与W的质量比为11∶9,且反应中消耗X的质量是生成W的质量的49,则反应中消耗Y的质量为()A.16gB.36gC.44gD.64g8.(2016?广安)物质X在4.8g氧气中恰好完全燃烧,反应方程式为X+3O2=====点燃RO2+2SO2,测得RO2和SO2的质量分别为2.2g和6.4g,下列判断中正确的是()A.参加反应的X的质量为4.3gB.X的相对分子质量为76C.X中含有R元素、S元素和O元素D.产物为气态时都是空气污染物9.(中考·河南)一定条件下,4.8gCH4与16.0gO2恰好完全反应,生成10.8gH2O、4.4gCO2和物质X,则X的质量为________g;该反应方程式中O2与X的化学计量数之比为________。训练角度四验证质量守恒定律(实验分析法)10.(2016·毕节改编)下列实验能验证质量守恒定律的是()11.(2015·宁夏改编)某同学用如图所示实验装置对质量守恒定律进行探究。请回答:(1)反应前,托盘天平的指针指向刻度盘的中央;那么,两种物质反应后,托盘天平的指针________(填“发生”或“不发生”)偏转。(2)你认为该同学的探究活动能否验证质量守恒定律?________。(3)如果你进行该探究活动,装置不变,你选用什么药品?____________________________。药品不变,你选用怎样的装置?_______________________。12.为了验证质量守恒定律,甲、乙、丙三位同学各做了一个实验:(1)甲同学用实验测定的数据有:木炭和坩埚的总质量为mg,其燃烧后灰烬和坩埚的总质量为ng,m和n的关系为:m________(填“>”“<”或“=”)n;(2)乙同学用实验测定的数据有:光亮的铁钉的质量为xg,其生锈后的质量为yg,x和y的关系为:x________(填“>”“<”或“=”)y;(3)丙同学实验测定的数据有:铁、硫酸铜溶液和烧杯的总质量为ag,其反应后的混合物和烧杯的总质量为bg,a与b的关系为:a________(填“>”“<”或“=”)b;(4)通过对三个实验的分析,你认为用有气体参加或生成的化学反应来验证质量守恒定律时,应________...