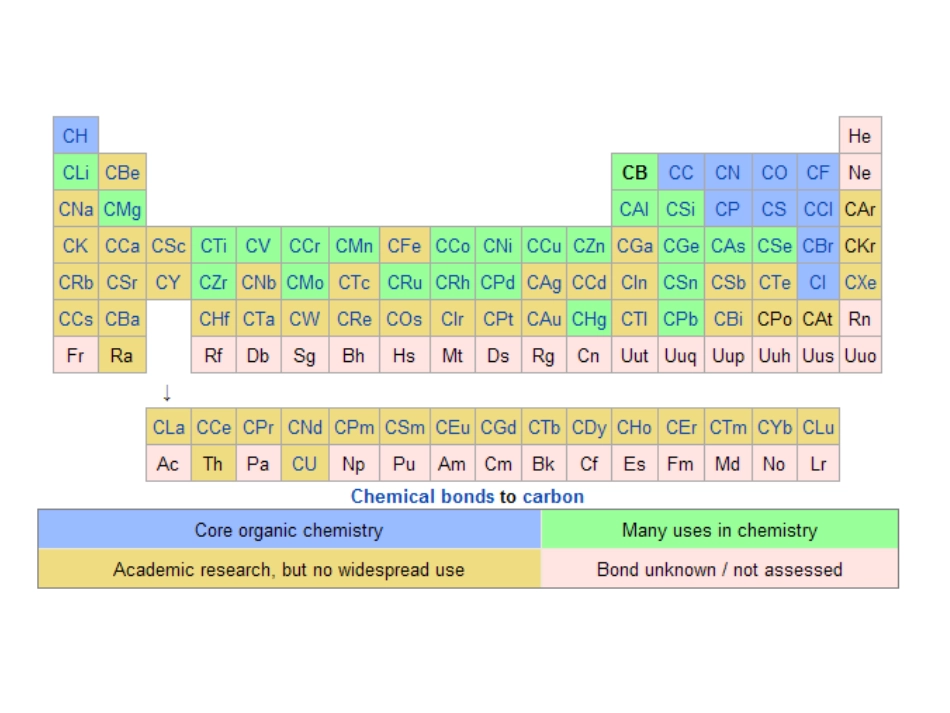
1第4章过渡金属有机化合物键配合物,σ键配合物;也包括:氢基配合物;以及N2,CO2,CS2,O2,PR3配合物等
本章要点:1
有效原子序数规则(18电子规则);2
过渡金属有机配合物的主要合成方法;3
过渡金属有机配合物的化学反应(基元反应)
34八隅体规则和有效原子序数规则•八隅体规则(Octetrule):金属价电子数与配体提供的电子数总和等于8的分子是稳定的
如PbEt4、二茂铍(Cp2Be)•有效原子序数规则(effectiveatomicnumberrule):金属的全部电子数与配体提供的电子数总和恰好等于金属所在周期中稀有气体的原子序数(如果只考虑价电子,金属价电子数与配体提供的电子数总和等于18)的分子是稳定的
此时亦称为18电子规则,如二茂铁
当然,也有例外
5配位数:配合物(包括络离子)与金属有机化合物中,中心原子的配位数是指与它结合的σ配位的原子数或π配位的电子对数
(徐光宪)符合18电子规则的配合物称为配位饱和;反之,成为配位不饱和
后过渡金属一般遵守,一些前过渡金属化合物和稀土金属配合物一般不遵守此规则
6茂五甲基茂茚基芴基718电子规则如何计算电子数:过渡金属外层的d、s轨道能量相近,容易发生d/s跃迁,人们往往将d电子和s电子的总和称之为d电子数
金属的价态、配体的种类和电子数:共价模型或离子模型,但不可混用
可以互相验证
这个规则仅是一个经验规则,不是化学键的理论
8中心金属的氧化态•MLn(metal-ligand)金属-配体•金属的氧化态:配体L以满壳层离开时,金属所保留的正电荷数e
M-Cl•烃基一般表现为负离子,所以把它们看成是负离子时,贡献为-1,e
M-CH3•中性配体(CO,H2C=CH2,PR3等)的贡献为零•环戊二烯基Cp为一价负离子•e
Cp2Fe,(Ph3P)3RhCl,Fe(CO)5,CH3Mn(C