高一化学离子反应【本讲主要内容】离子反应本节是中学化学重要的基本概念,主要内容是让同学们了解电解质和非电解质,强电解质和弱电解质的概念,理解离子反应和离子方程式的含义,理解离子反应发生的条件和离子方程式的书写方法,能根据离子反应的规律判断一些常见离子在同一溶液中能否共存、离子方程式是否正确等问题
【知识掌握】【知识点精析】前面,我们复习了化学反应的四大基本类型,并且学习了氧化还原反应,知道根据研究问题的角度不同,化学反应可有不同的分类方式
那么今天我们将继续学习另外一种重要的分类方法,将有离子参加的反应统称为离子反应,没有离子参加的反应叫做非离子反应
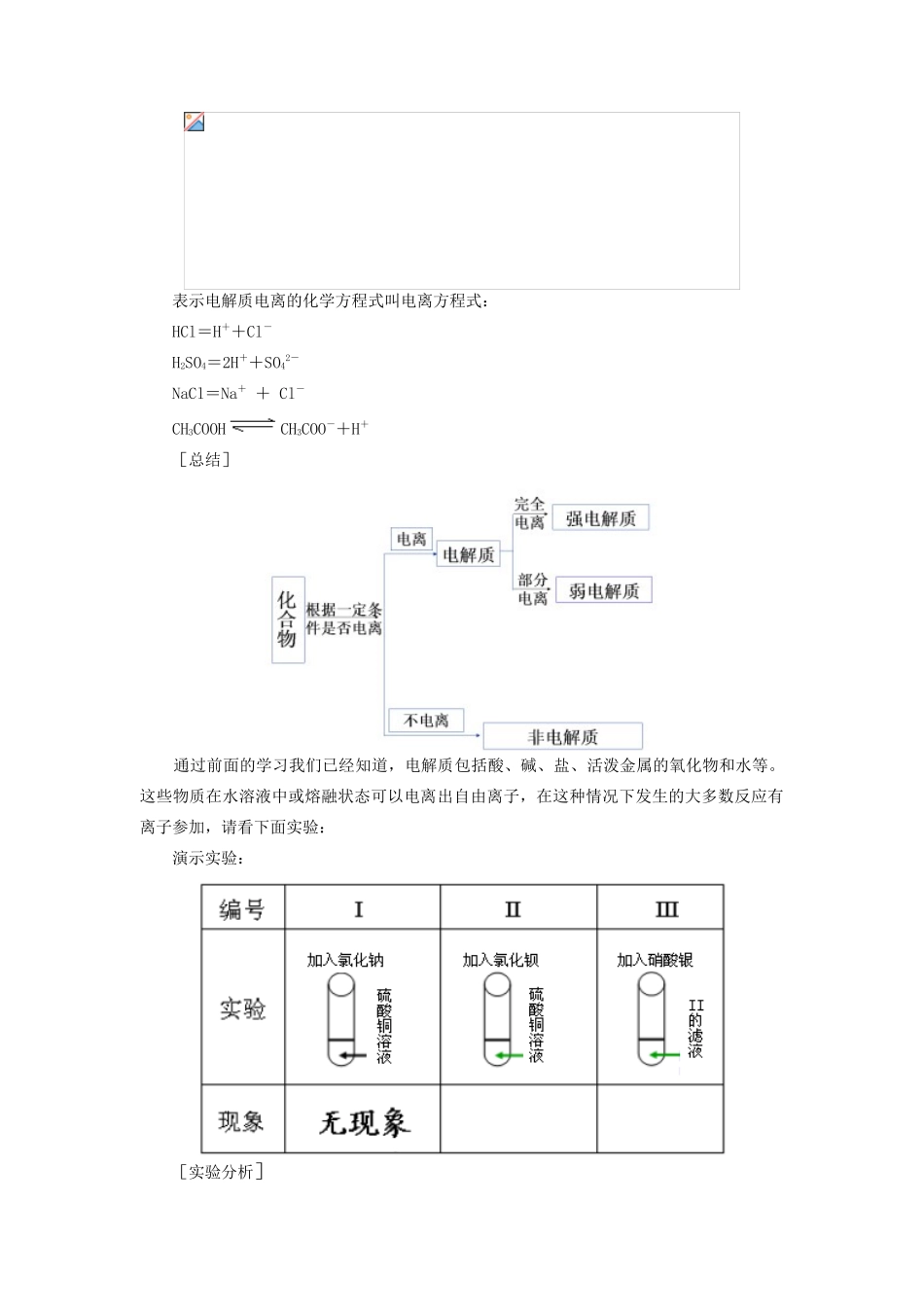
下面,我们就来学习离子反应,见如下实验装置图:通过实验我们会发现溶液导电性不同
用盐酸、氢氧化钠、氯化钠溶液进行实验时,灯泡明亮;醋酸、氨水做实验时灯泡较暗;而用酒精进行实验时灯泡不亮
在初中我们已经了解了溶液导电是靠自由移动的离子,于是我们把化合物在一定的条件下离解成自由移动离子的过程叫做电离,而根据化合物的电离的不同我们可将化合物分成电解质和非电解质
我们把这种在水溶液里或熔融状态下能够导电的化合物叫做电解质,如:酸、碱、盐
[讨论]下列物质中哪些是电解质
Cu、NaCl固体、NaOH固体、K2SO4溶液、CO2、蔗糖、NaCl溶液、H2O、酒精
[小结]应注意以下几点:①电解质应是化合物
而Cu则是单质,K2SO4与NaCl溶液都是混合物
②电解质应是一定条件下本身电离而导电的化合物
而CO2能导电是因CO2与H2O反应生成了H2CO3,H2CO3能够电离而非CO2本身电离
所以CO2不是电解质
③酸、碱、盐、水是电解质,蔗糖、酒精为非电解质
通过上面的实验我们还发现,相同条件下,不同种类的酸、碱、盐溶液的导电能力也不相同
电解质溶液导电能力的大小决定于溶液中自由移动的离子的浓度和离子所带电荷数
而当溶液体积、浓度和离子