第6天(物质分类、胶体、电解质、电离)【学习目标】1.了解物质分类的方法及胶体的性质
2.学会判断电解质、非电解质;能够书写电离方程式
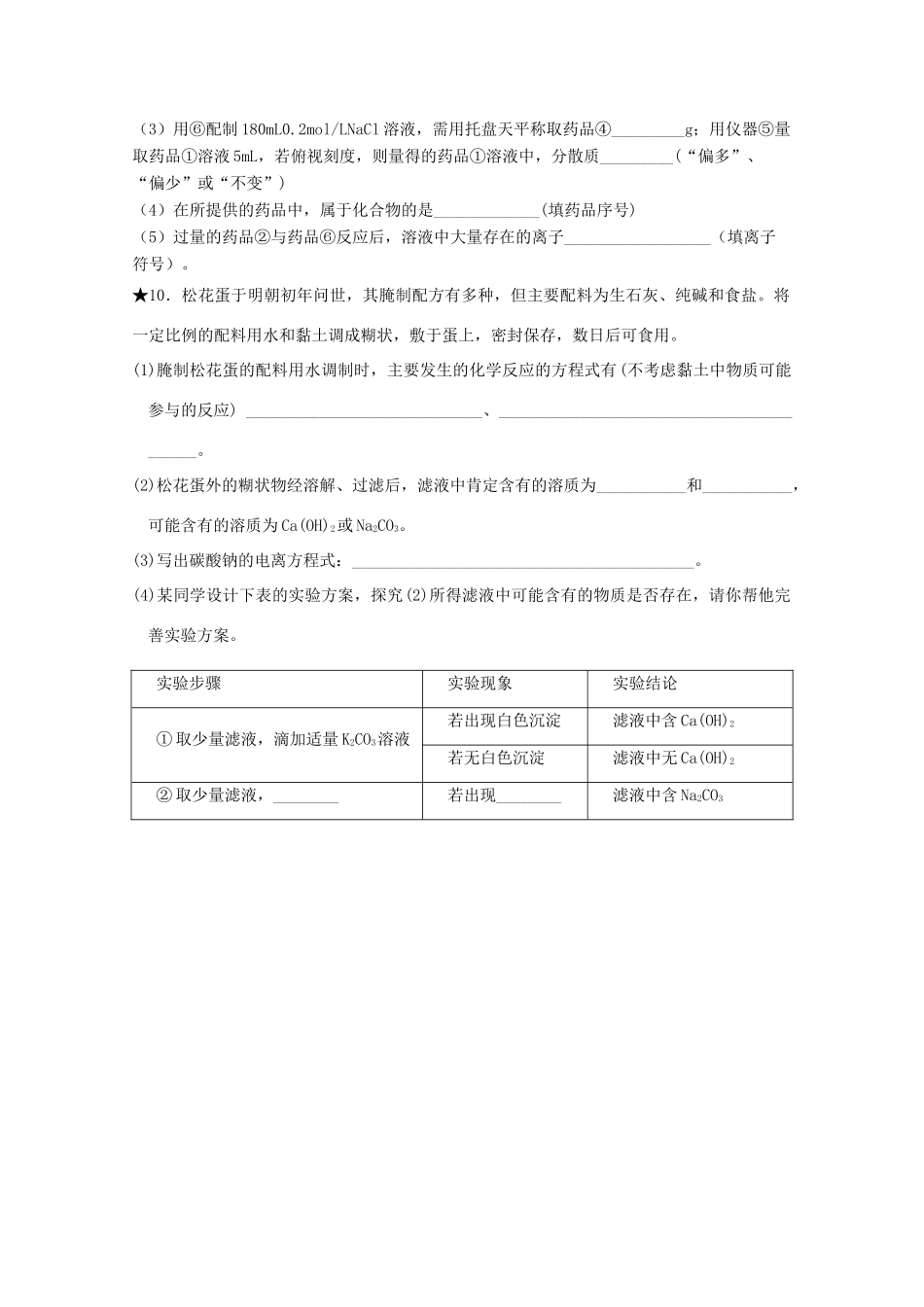
【本日作业】一、选择题(共8题,每题只有一个正确答案)1.下列关于物质的分类的说法正确的是()A.据含有的元素的类别可将氧化物分为金属氧化物和非金属氧化物B.化合物可以分为酸、碱、盐三类C.HNO3从不同的角度分类,其分别属于含氧酸、一元酸和弱酸D.据能否溶于水可将物质分为易溶和难溶两类2.某学生以铁丝和Cl2为原料进行下列三个实验
从分类角度分析,下列选项正确的是()A.实验①、②所涉及的物质均为电解质B.实验②得到浅绿色溶液C.实验③长时间加热会得到红褐色沉淀D.实验①、②、③均为离子反应3.下列有关胶体这种分散系的说法不正确的是()A.胶体是一类类似果冻状的混合物B.制备Fe(OH)3胶体的化学方程式为:FeCl3+3H2O====Fe(OH)3(胶体)+3HClC.制得的Fe(OH)3胶体分散质粒子直径大小在1nm~100nm之间D.Fe(OH)3胶体与CuSO4溶液可以利用丁达尔效应加以区分4.下列物质属于电解质的是()A.CuB.乙醇C.CH3COOHD.KNO3溶液5.设NA为阿伏加德罗常数,下列对0
3mol/L硫酸钾溶液的不正确说法是()A.1L溶液中含有0
3NA个钾离子B.1L溶液中含有钾离子和硫酸根离子总数为0
9NAC.2L溶液中钾离子的浓度为0
6mol/LD.2L溶液中含有0
6NA个硫酸根离子6.水溶液中下列物质的电离方程式正确的是()A.Al2(SO4)3===Al3++SO42-B.NaHCO3===Na++H++CO32-C.Ba(OH)2===Ba2++(OH)2-D.NaHSO4===Na++H+SO42-7.下列说法正确的是()A.碱石灰是强电解质B.HClO是弱酸,但NaClO是强电解质C.KC