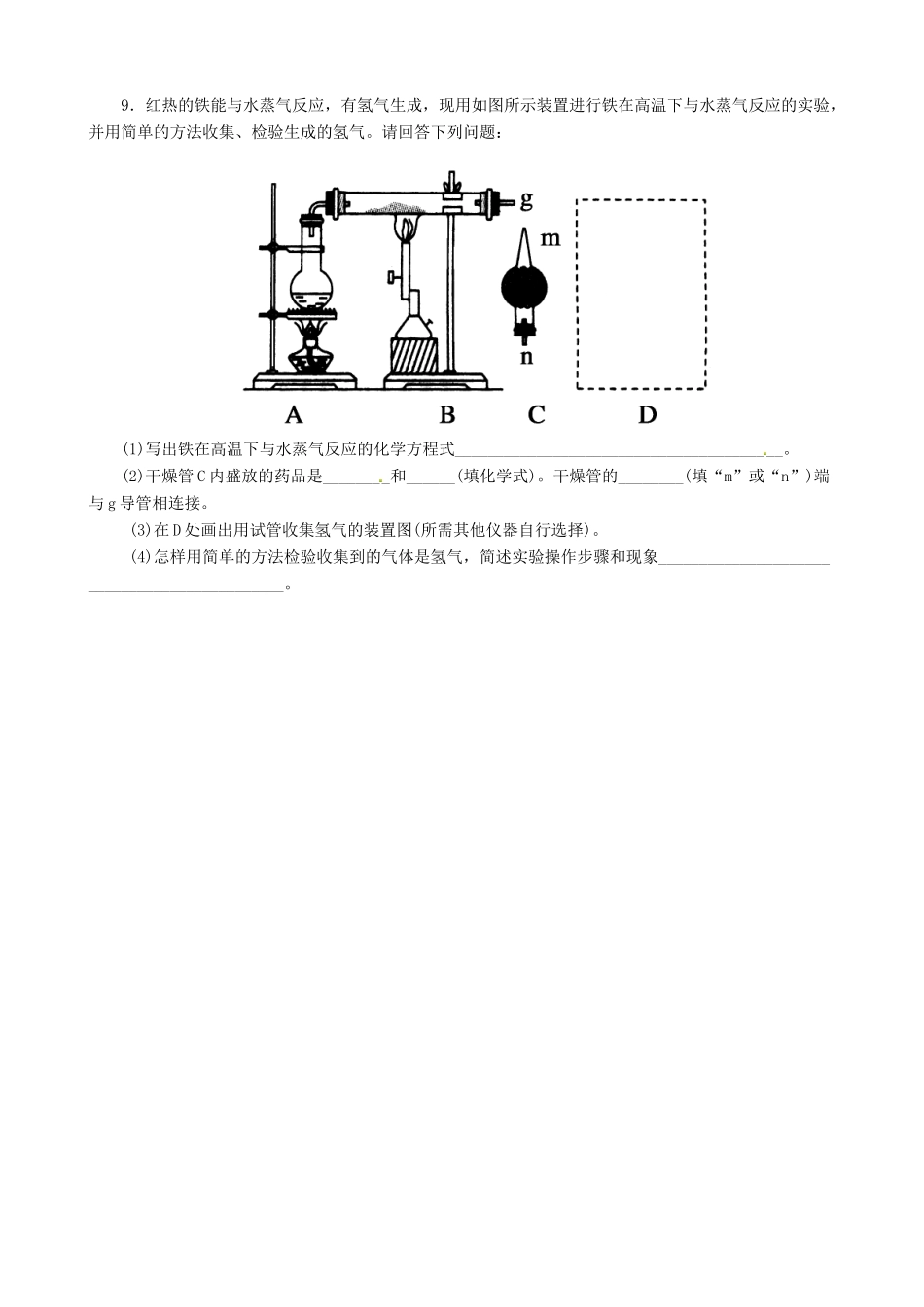
3.1金属的化学性质1.下列关于金属钠的叙述中正确的是()A.钠在空气中能发生缓慢氧化而自燃B.金属钠可保存在煤油中,也可保存在CCl4中C.钠能和CuSO4溶液反应置换出CuD.钠投入到水中立即熔化成小球,说明其熔点低,且钠与水的反应是放热反应2.下列关于金属铝的叙述中,说法不正确的是()A.Al是地壳中含量最多的金属元素B.Al是比较活泼的金属,在化学反应中容易失去电子,表现还原性C.铝箔在空气中受热可以熔化,且发生剧烈燃烧D.铝箔在空气中受热可以熔化,由于氧化膜的存在,熔化的Al并不滴落3.等质量的钠、镁、铝分别与足量的盐酸反应,产生H2的质量由大到小的排列顺序正确的是()A.Al、Mg、NaB.Mg、Al、NaC.Na、Mg、AlD.Na、Al、Mg4.下列反应的离子方程式书写正确的是()A.钠和水反应:Na+H2O===Na++OH-+H2↑B.钠投入足量盐酸中:2Na+2H+===2Na++H2↑C.铁和稀硫酸反应:2Fe+6H+===2Fe3++3H2↑D.钠投入氯化铁溶液中:3Na+Fe3+===3Na++Fe5.下列说法中,错误的是()A.钠在空气中加热时,先熔化,再燃烧,燃烧所得产物为Na2O2B.镁因在空气中形成一薄层致密的氧化膜保护了里面的镁,故镁不需要像钠一样做特殊保护C.铝制品在生活中非常普遍,是因为铝不活泼D.铁因在潮湿的空气中生成的氧化物疏松多孔,不能保护内层金属,故铁制品往往需要加保护层6.将少量金属钠分别投入下列物质的水溶液中,有气体放出,且溶液质量减轻的是()A.HClB.NaOHC.K2SO4D.CuSO47.将2.3g金属钠投入100g水中,反应结束后,下列表示的溶液中溶质的质量分数计算式中,正确的是()A.×100%B.×100%C.×100%D.×100%8.有A、B、C三种常见的金属单质,A在空气中燃烧生成淡黄色固体;B也能在空气中剧烈燃烧,发出耀眼的白光;C在一定条件下与水蒸气反应生成H2和一种黑色固体。根据以上信息回答下列问题:(1)写出化学式A___________;B___________;C____________。(2)写出化学方程式①A在空气中燃烧______________;②C与水蒸气反应_____________________________________;③A与水反应________________________________________。9.红热的铁能与水蒸气反应,有氢气生成,现用如图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气。请回答下列问题:(1)写出铁在高温下与水蒸气反应的化学方程式________________________________________。(2)干燥管C内盛放的药品是________和______(填化学式)。干燥管的________(填“m”或“n”)端与g导管相连接。(3)在D处画出用试管收集氢气的装置图(所需其他仪器自行选择)。(4)怎样用简单的方法检验收集到的气体是氢气,简述实验操作步骤和现象_____________________________________________。课堂练习1.D。钠在空气中能发生缓慢氧化但不会自燃;钠的密度小于CCl4的密度,不能保存在CCl4中;钠放入CuSO4溶液中,钠先与水发生反应生成NaOH,NaOH可与CuSO4发生反应生成Cu(OH)2蓝色沉淀,不会将Cu置换出来;钠与水反应放热且钠熔点低,故钠熔化成小球。2.C。Al是活泼金属,其原子结构为,易失去最外层电子,有较强的还原性,Al的熔点较低(660℃),但其氧化物的熔点很高(2050℃),所以铝箔加热时,Al熔化,但被氧化膜包住不会滴落。3.A。金属与酸反应要先比较金属与酸的量,应按少量的物质计算产生H2的量。因与足量的盐酸反应,则金属全部反应产生H2。根据电子得失守恒,Na、Mg、Al产生的H2分别为×1、×2、×3。故产生H2的质量由大到小应为Al、Mg、Na。4.B。A项,配平错误;C项,铁与酸反应生成的是Fe2+;D项,Na会与水反应,所以在溶液中不能置换出其他金属。5.C。6.D。在A、B、C三个选项中只有H2放出,故溶液质量是增加的。D选项中由于Na与H2O反应生成的NaOH还能继续与CuSO4反应析出Cu(OH)2沉淀:2Na+CuSO4+2H2O===Cu(OH)2↓+Na2SO4+H2↑,故反应后溶液质量减轻。7.B。2.3g钠投入水中产生的氢氧化钠为4g,产生的氢气为0.1g,即溶质为4g,溶液质量为(100+2.3-0.1)g。8.(1)NaMgFe(2)①2Na+O2Na2O2②3Fe+4H2O(g)Fe3O4+4H2③2Na+2H2O===2NaOH+H2↑9.解析:本题以氢气的干燥、收集、检验为...