电离时能产生金属阳离子 ( 或铵根离子 ) 和酸根阴离子的化合物,叫做盐
盐是酸跟碱中和的产物
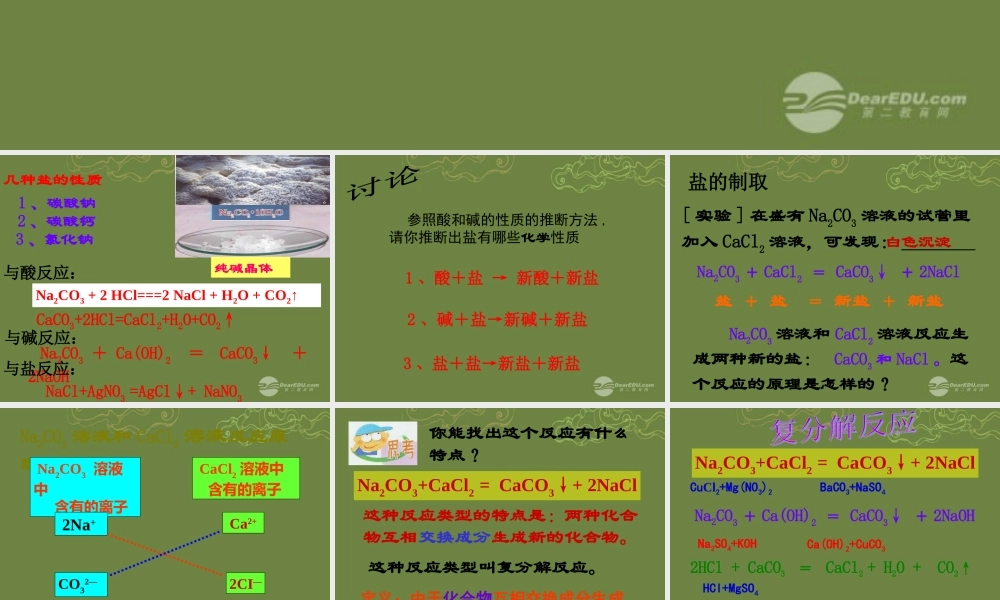
几种盐的性质 1 、碳酸钠纯碱晶体与酸反应:Na2CO3 + 2 HCl===2 NaCl + H2O + CO2↑与碱反应: Na2CO3 + Ca(OH)2 = CaCO3↓ +2NaOH2 、碳酸钙CaCO3+2HCl=CaCl2+H2O+CO2↑3 、氯化钠NaCl+AgNO3 =AgCl↓+ NaNO3与盐反应: 1 、酸+盐 → 新酸+新盐 2 、碱+盐→新碱+新盐 3 、盐+盐→新盐+新盐 参照酸和碱的性质的推断方法 ,请你推断出盐有哪些化学性质[ 实验 ] 在盛有 Na2CO3 溶液的试管里加入 CaCl2 溶液,可发现: ________白色沉淀 Na2CO3 + CaCl2 = CaCO3↓ + 2NaCl Na2CO3 溶液和 CaCl2 溶液反应生成两种新的盐: CaCO3 和 NaCl
这个反应的原理是怎样的
盐 + 盐 = 新盐 + 新盐盐的制取Na2CO3 溶液和 CaCl2 溶液反应原理 Na2CO3 溶液中 含有的离子 CaCl2 溶液中 含有的离子 2Na+CO32— Ca2+2CI—Na2CO3+CaCl2 = CaCO3↓+ 2NaCl你能找出这个反应有什么特点
这种反应类型的特点是:两种化合物互相交换成分生成新的化合物
定义:由于化合物互相交换成分生成新化合物的反应叫复分解反应
这种反应类型叫复分解反应
Na2CO3+CaCl2 = CaCO3↓+ 2NaClNa2CO3+CaCl2 = CaCO3↓+ 2NaCl Na2CO3 + Ca(OH)2 = CaCO3↓ + 2NaOH2HCl + CaCO3 = CaCl2 + H2O + CO2↑Ca(OH)2+CuCO3HCl+MgSO4 CuCl2+Mg(NO3)2BaCO3+N