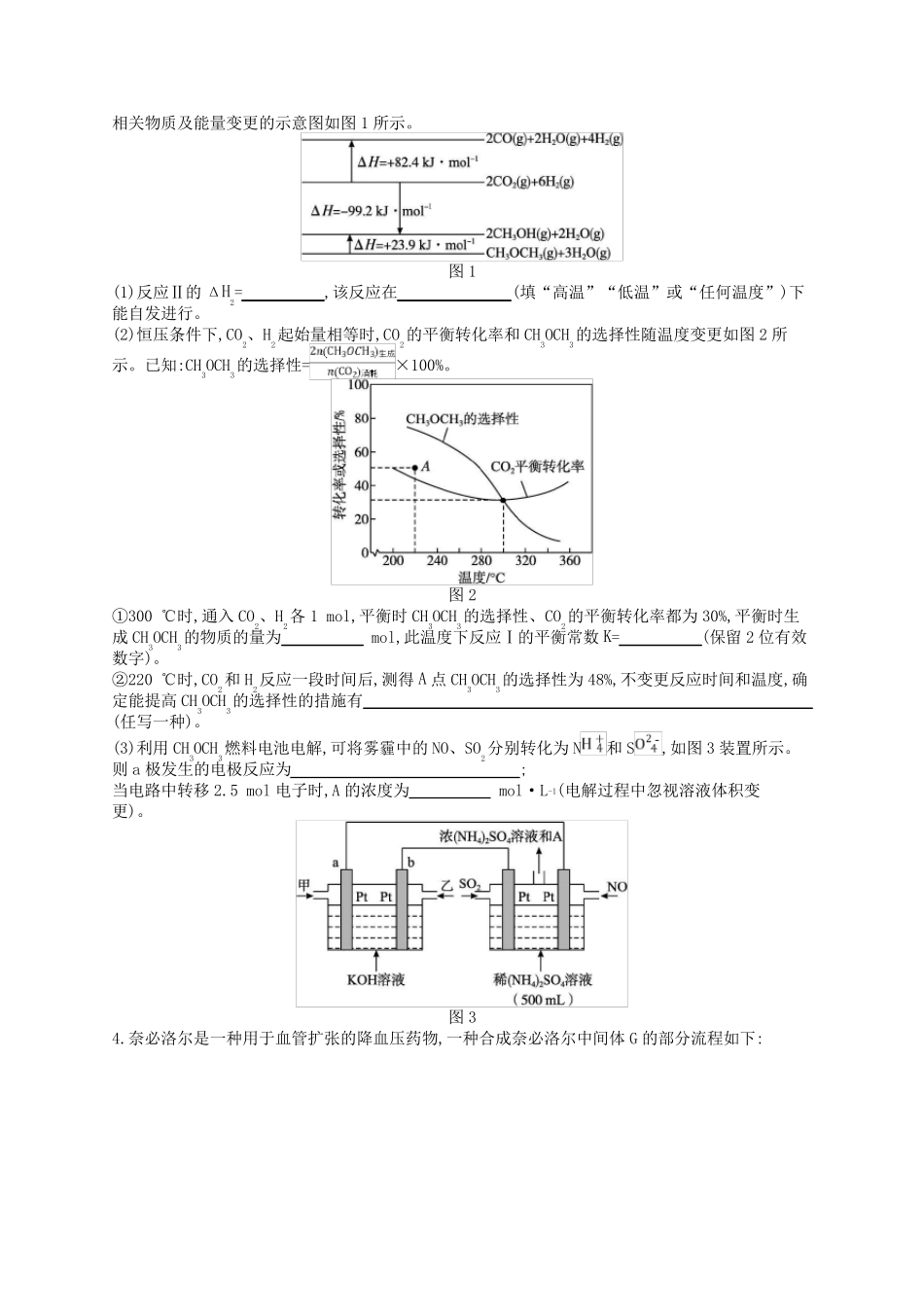
非选择题专项练四 1
某学习小组将Cu 与H2O2的反应设计为原电池,并进行相关试验探究
回答下列问题: Ⅰ
试验打算 (1)稀硫酸的配制 ①配制100 mL 0
3 mol·L-1的H2SO4溶液,需6 mol·L-1 H2SO4溶液的体积为 mL
②在试验室配制上述溶液的过程中,下图所示仪器,须要用到的是 (填仪器名称)
(2)Cu 与H2O2在酸性条件下反应的离子方程式为
试验探究 【试验任务】利用相关原电池装置进行试验,探究物质氧化性或还原性的影响因素
【查阅资料】其他条件相同时,参加原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大
【进行试验】 (3)利用下表所示装置进行试验1~4,记录数据
装置 试验序号 烧杯中所加试剂 电压表读数 30% H2O2 0
3 mol·L-1 H2SO4 H2O V/mL V/mL V/mL 1 30
0 — 10
0 U1 2 30
0 U2 3 30
0 U3 4 35
0 V1 U4 已知:本试验条件下,S对电压的影响可忽视
①依据表中信息,补充数据:V1=
②由试验2 和4 可知,U2 (填“大于”或“小于”或“等于”)U4,说明其他条件相同时,H2O2溶液的浓度越大,其氧化性越强
(4)由(3)中试验结果U3>U2>U1,小组同学对“电压随pH 减小而增大”可能的缘由,提出了以下两种猜想: 猜想1:酸性条件下,H2O2的氧化性随pH 减小而增加
猜想2:酸性条件下,Cu 的还原性随pH 减小而增加
为验证猜想,小组同学在(3)中试验1~4 的基础上,利用下表装置进行试验5~7,并记录数据
装置 试验序号 操作 电压表读数 5 — U5 6 ①向 (填“左”或“右”)侧烧杯中滴加5
0 mL 0
3 mol·L-1 H2SO4溶