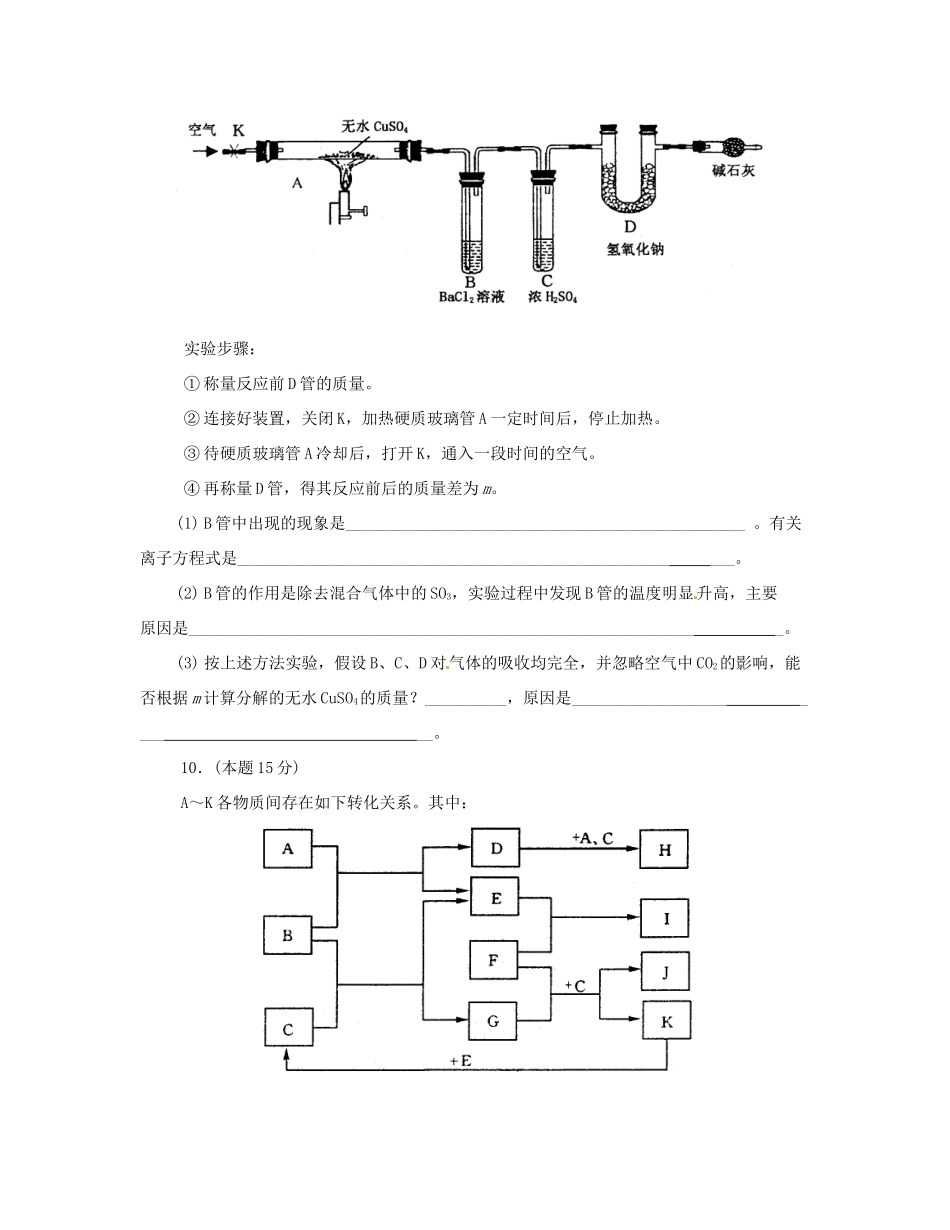
四川省德阳五中高三化学综合练习6(50分钟完卷,满分108分)可能用到的相对原子质量:H 1 N 14 O 16 Ne 20 1.如果取一块冰放在容器里,不断地升高温度,可以实现“冰→水→水蒸气→氢气和氧气”的变化,在各步变化时破坏的粒子间的相互作用依次是A.氢键、极性键、非极性键B.氢键、氢键、极性键C.氢键、氢键、非极性键D.氢键、非极性键、极性键2.广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果都是参与反应的物质和水分别离解成两部分,再重新组合成新的物质
根据上述观点,下列说法不正确的是A.NaClO 的水解产物是 HClO 和 NaOH B.CuCl2的水解产物是 Cu(OH)2和 HClC.PCl3的水解产物是 PH3和 HClD.CaO2的水解产物是 Ca(OH)2和 H2O23.下列说法正确的是A.不用其它试剂便无法区别 NaCl、Na2CO3、NaHSO4、AlCl3四种溶液B.实验室常用带玻璃塞的试剂瓶保存 NaOH 溶液C.用导线将电解池和电池连接,电子从电池的负极流向电解池的阳极D.用以下反应制取硫酸铜:2Cu + O2 2CuO、 CuO + H2SO4 = CuSO4 + H2O,符合绿色化学的理念4.几种短周期元素的原子半径和主要化合价见下表:元素代号XYZLMQ原子半径/nm0
074主要化合价+ 2+ 3+ 6、– 2 + 7、– 1+ 4、– 4– 2下列说法正确的是A.在化学反应中,M 原子既不容易失去电子,又不容易得到电子B.等物质的量的 X、Y 的单质与足量盐酸反应,生成 H2一样多C.Y 与 Q 形成的化合物不可能跟氢氧化钠溶液反应△D.Z 的氢化物的稳定性强于 L 的氢化物的稳定性5.NA为阿伏加德罗常数
下列叙述中正确的是A.1L 1 mol/L 醋酸溶液中的离子总数