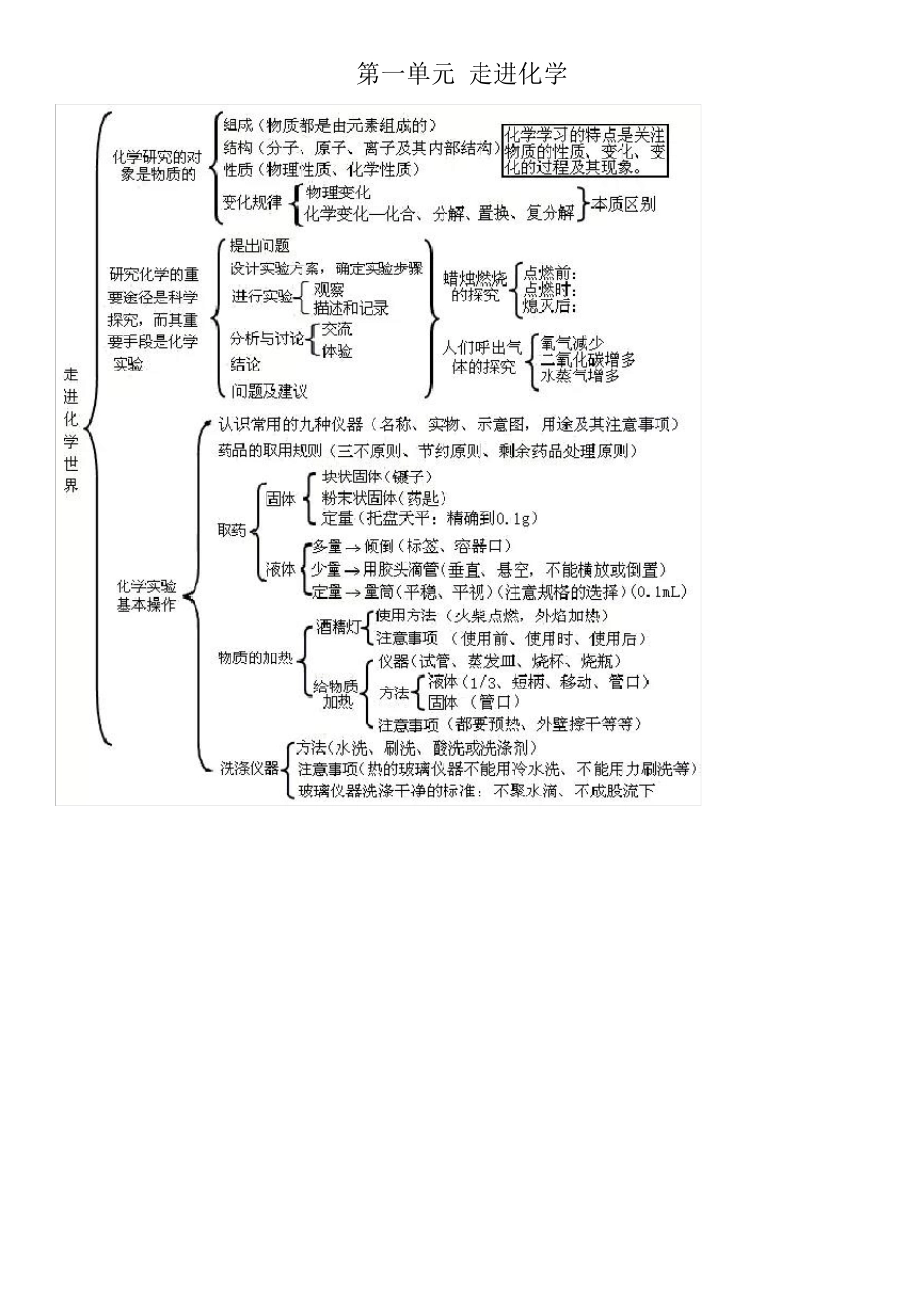
第一单元 走进化学 第二单元 我们周围 第三单元 物质的构成 第四单元 自然界的水 第五单元 化学方程式 第六单元 碳和碳的氧化物 第七单元 燃烧及其 第八单元 金属和金属材料 第九单元 溶液 第十单元 酸、碱、盐 一 、化学用语 1、电离方程式 2、物质的俗称和主要成分: 生石灰 CaO;熟石灰、消石灰、石灰水的主要成分 Ca(OH)2;石灰石、大理石 CaCO3;食盐的主要成分 NaCl ;纯碱、口碱 Na2CO3;烧碱、火碱、苛性钠 NaOH;胆矾、蓝矾 CuSO4.5H2O;碳酸钠晶体 Na2CO3.10H2O;氨水 NH3.H2O; 二、金属活动性 1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au 2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。 3、金属活动性顺序的应用: (1)排在氢前的金属能置换出酸里的氢(元素)。 (2)排 在 前 面 的 金 属 才 能 把 排 在 后 面 的 金 属 从 它 们 的 盐 溶 液 中 置 换 出 来 (K、 Ca、 Na 除 外 )。 三 、酸、碱、盐的溶解性 1、 常 见 盐 与 碱 的 溶 解 性 : 钾 (盐 )、 钠 (盐 )、 铵 盐 全 都 溶 , 硝 酸 盐 遇 水 影 无 踪 。 硫 酸 盐 不 溶 硫 酸 钡 , 氯 化 物 不 溶 氯 化 银 。 碳 酸 盐 只 溶 钾 (盐 )、 钠 (盐 )、 铵 (盐 )。 碱 类 物 质 溶 解 性 : 只 有 (氢 氧 化 )钾 、 (氢 氧 化 )钠 、 (氢 氧 化 )钙 、 (氢 氧 化 )钡 溶 。 2、 八 个 常 见 的 沉 淀 物 : 氯 化 银 、 硫 酸 钡 碳 酸 银 、 碳 酸 钡 、 碳 酸 钙 、 氢 氧 化 镁 、 氢 氧 化 铜 、 氢 氧 化 铁 3、 四 微 溶 物 : Ca(OH)2(石 灰 水 注 明 “澄清”的 原因)、 CaSO4(实验室制二氧 化 碳 时不 用稀硫 酸 的 原因) Ag2SO4(鉴别 SO42-和 Cl-时, 不 用硝 酸 银 的 原因)、 MgCO3(碳 酸 根离子不 能 用于在 溶 液 中 除 去镁 离子的 原因) 4、 三个 不 存在 的 物 质 : 氢 氧 化 银 、 碳 酸 铝、 碳 酸 铁 四、复分解反应发生的条件反应: 有 气体、 水 或沉 淀 生成(即有 不 在 溶 液 中 存在 或在 水 溶 液 中 不 易电...