课题一 原子的构成历史1 、 公元前 5 世纪,希腊哲学家德谟克利特等人认为 :万物是由大量的不可分割的微粒构成的,即原子
19 世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体
1897 年,英国科学家汤姆生发现了电子
卢瑟福原子模型问题• 1
原子的特点是什么
• 原子是化学变化中的最小粒子原子原子核核外电子质子中子3
质子、中子、电子的电性和电量怎样
1 个质子带一个单位正电荷;1 个电子带一个单位负电荷
中子不带电;1 个质子带 1 个单位正电荷,中子不带电,因此原子核带正电荷
原子核所带的正电荷数目叫做核电荷数,它在数值上等于原子核所含的质子数目
原子种类原子核核外电子数核电荷数质子数 中子数氢1101碳6666氧8888钠11111211铁26263026从表中可以得出:1 、原子中,质子数=核外电子数;2 、核内质子数就是核电荷数;3 、质 子 数 不 一 定 等 于 中 子 数,原 子 中 不 一 定 含 有 中 子;4 、构成原子的必要粒子是质子和电 子,决定原子种类的是核内质子数, 它必不可少
即是:核电荷数=质子数=核外电子数问题:铁、铜等金属都是原子直接构成的,原子中存在带电荷的粒子(质子和电子),原子是否显电性
实验 1 、用手接触铁、铜等金属是否会触 电
2 、用电工的电笔测铁、铜是否带电
在原子中,由于质子(原子核)与电子所带电荷数相等,但电性相反,所以整个原子不显电性
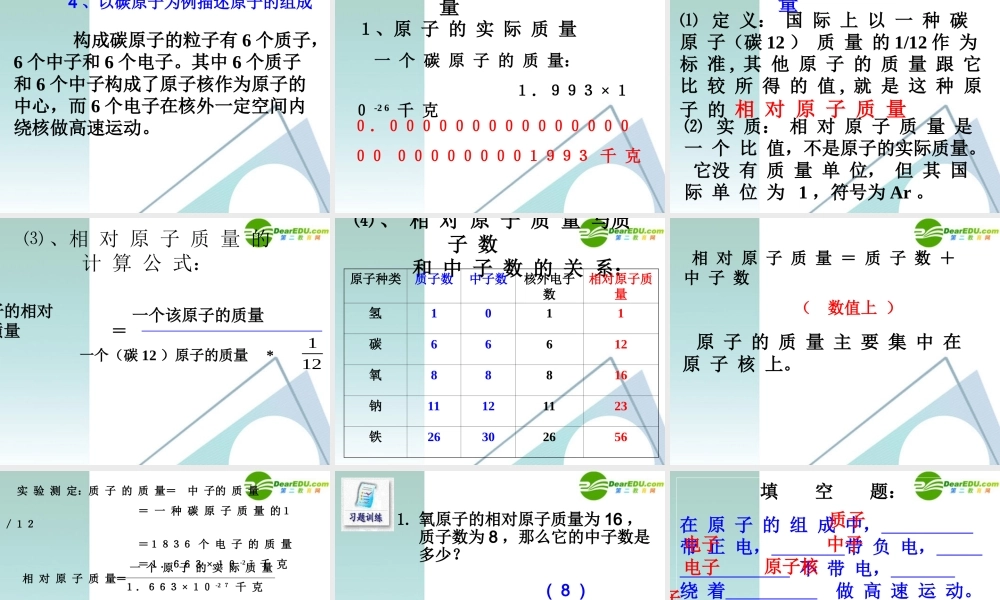
原子不显电性的原因:4 、以碳原子为例描述原子的组成 构成碳原子的粒子有 6 个质子,6 个中子和 6 个电子
其中 6 个质子和 6 个中子构成了原子核作为原子的中心,而 6 个电子在核外一定空间内绕核做高速运动
二、 相 对 原 子 质 量 一 个 碳 原 子 的 质 量: 1.993 × 10 -2 6 千 克 1、原 子 的