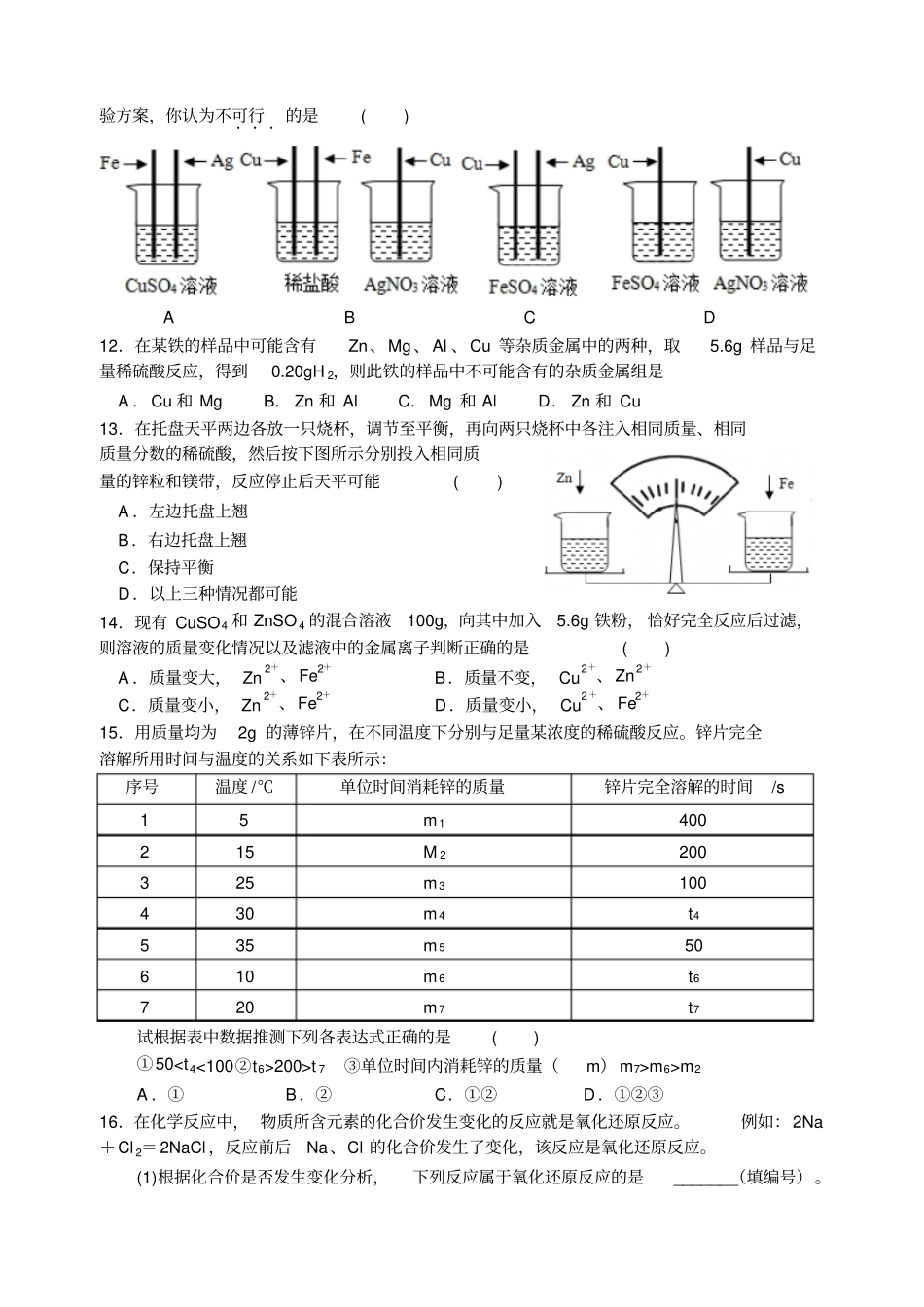
《金属的冶炼与利用》培优专题练习【金属的化学性质 】1.为探究Zn 和 Cu 的金属活动性强弱,提供的试剂有:Zn、Cu、H 2SO4 溶液、 ZnSO4溶液、 CuSO4溶液。下列说法正确的是( ) A .选用两种试剂可实现实验目的B.ZnSO4 溶液中加入Cu 不能探究金属活动性强弱C.最多只能设计一种实验方案D.根据 Zn 和 Cu 的硬度能判断金属活动性强弱2.R 为金属,发生如下反应:R+CuSO4=Cu+RSO4。下列说法错误的是( ) A .该反应为置换反应B.R 的金属活动性比Cu 强C.该金属可以是Al D.若 R 为 Fe,反应后溶液的质量会减小3.废旧手机的某些部件中含有Mg 、Al 、 Cu、Ag 等金属,为了回收重金属,将旧手机的部件粉碎并浸入足量稀硫酸中充分反应后过滤,所得固体中含有的金属是( ) A .Mg、 Al B.Cu、 Ag C.Al 、 Cu D.Mg 、Ag 4.医用热敷袋使用时要轻揉,袋内的反应可看作是铁粉、空气和水相互作用,产生氢氧化亚铁,最终转化为氢氧化铁。下列说法错误的是( ) A .热敷袋放出的热量是由化学反应产生的B.总反应为2Fe+O2+3H 2O= 2Fe(OH) 3C.上述含铁物质中铁元素的化合价有0、+ 2、+ 3 D.热敷袋中的铁粉与水在未使用时要分别密封保存5.有甲、乙、丙三种金属,只有甲在自然界中主要以单质形式存在,丙的盐溶液不能用乙制的容器盛放,则这三种金属的活动性由强到弱的顺序是( ) A .甲 >乙>丙B.丙 >乙>甲C.丙 >甲 >乙D.乙 >丙>甲6.将等质量的镁、铁、锌分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2 质量与反应时间的关系如图所示。根据图中的信息,作出的判断不正确的是( ) A .图线 X 表示镁的反应情况B.铁消耗的稀盐酸质量最大C.镁、锌一定过量,铁可能反应完D.镁一定过量,锌、铁可能反应完7.在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。(1)CuSO 4 溶液中,大量存在的离子是_______。(2)小明同学将一根久置于空气中的铝丝插入CuSO4 溶液中, 未见任何明显现象,小明马上明白原因是____________________________ 。于是他将铝丝经过_______处理后再次浸入到 CuSO4 溶液中,静置,观察到的现象是_____________________。结合现象分析,溶液中减少的离子是_______,增加的离子是_______。(3)除 CuSO4 溶液外,将铝丝浸入_______(任举一例)溶液中,也能产生相同的实验现象。8.在课外活动中,老师要求学生...