高二化学自编作业——化学平衡综合应用练习1.[2014·新课标全国卷Ⅰ,有删减]乙醇是重要的有机化工原料,可由乙烯气相直接水合法生产或间接水合法生产
回答下列问题:(1)已知:甲醇的脱水反应:2CH3OH(g)===CH3OCH3(g)+H2O(g)ΔH1=-23
9kJ·mol-1甲醇制烯烃的反应:2CH3OH(g)===C2H4(g)+2H2O(g)ΔH2=-29
1kJ·mol-1乙醇的异构化反应:C2H5OH(g)===CH3OCH3(g)ΔH3=+50
7kJ·mol-1则乙烯气相直接水合反应C2H4(g)+H2O(g)===C2H5OH(g)的ΔH=____________________kJ·mol-1
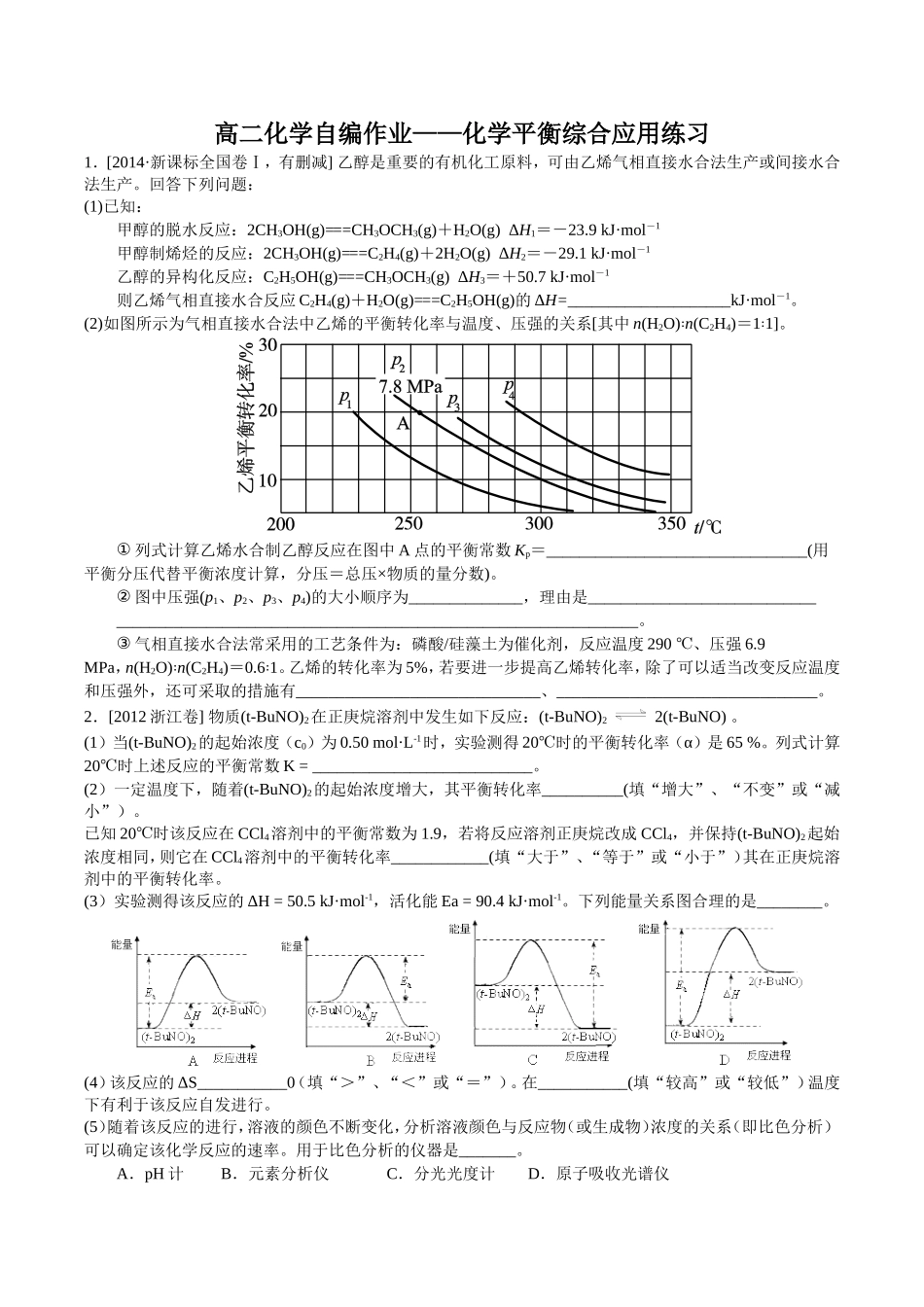
(2)如图所示为气相直接水合法中乙烯的平衡转化率与温度、压强的关系[其中n(H2O)∶n(C2H4)=1∶1]
①列式计算乙烯水合制乙醇反应在图中A点的平衡常数Kp=________________________________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
②图中压强(p1、p2、p3、p4)的大小顺序为______________,理由是____________________________________________________________________________________________
③气相直接水合法常采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290℃、压强6
9MPa,n(H2O)∶n(C2H4)=0
乙烯的转化率为5%,若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可采取的措施有______________________________、________________________________
2.[2012浙江卷]物质(t-BuNO)2在正庚烷溶剂