高考总复习《氮磷》【考纲要求】1.了解氮气的性质及应用
2.了解氮的氧化物(NO、NO 2)的性质及对环境的影响
3.掌握氨气的结构、性质、制法和用途
4.了解硝酸的氧化性
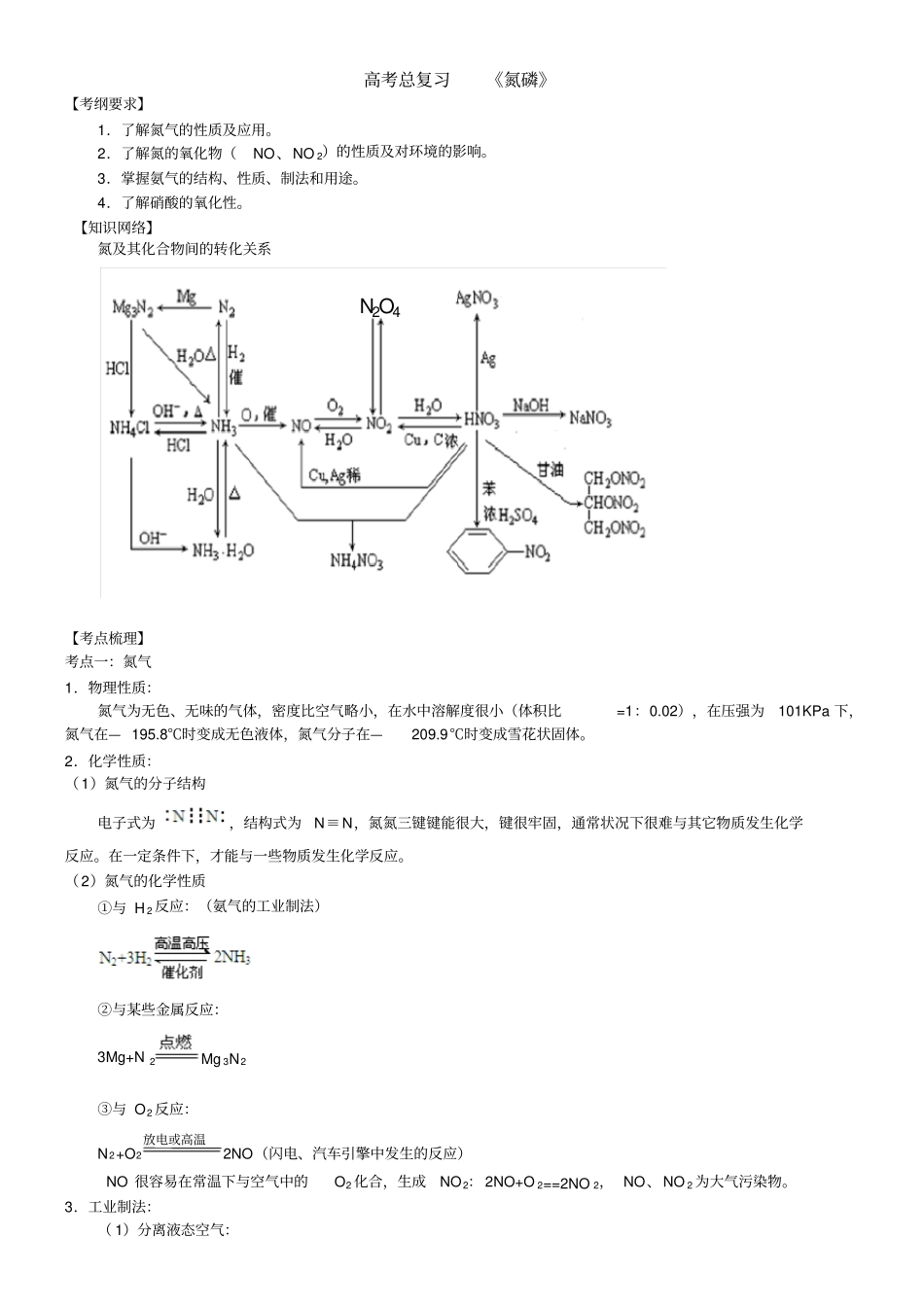
【知识网络】氮及其化合物间的转化关系N2O4【考点梳理】考点一:氮气1.物理性质:氮气为无色、无味的气体,密度比空气略小,在水中溶解度很小(体积比=1:0
02),在压强为101KPa 下,氮气在— 195
8℃时变成无色液体,氮气分子在—209
9℃时变成雪花状固体
2.化学性质:(1)氮气的分子结构电子式为,结构式为N≡N,氮氮三键键能很大,键很牢固,通常状况下很难与其它物质发生化学反应
在一定条件下,才能与一些物质发生化学反应
(2)氮气的化学性质①与 H 2 反应:(氨气的工业制法)②与某些金属反应:3Mg+N 2Mg 3N2③与 O2 反应:N2+O2放电或高温2NO(闪电、汽车引擎中发生的反应)NO 很容易在常温下与空气中的O2 化合,生成NO 2: 2NO+O 2==2NO 2, NO、NO 2 为大气污染物
3.工业制法:( 1)分离液态空气:( 2)耗氧法:4.用途:工业原料,合成氨,制化肥,HNO 3,保护气,致冷剂考点二:二氧化氮和一氧化氮的比较【高清课堂: 356211 氮的氧化物】NO NO 2物理性质色态味无色、无味、气体红棕色、刺激性气味、气体密度密度略大于空气密度比空气大,熔沸点很低低,易液化溶解性不溶易溶毒性有毒有毒化学性质与水不反应3NO 2+H 2O=2HNO 3+NO NO 2 既是氧化剂,又是还原剂与碱不反应2NO 2+2NaOH=NaNO 3+NaNO 2+H2O NO +NO 2 +2NaOH=2NaNO 2 +H 2O 氧化性2NO+2CO=2CO 2+N 22NO 2+2KI=I 2+2KNO 2还原性2NO+O 2=2NO 2可使 KMnO 4 褪色可