实 用 文 档1 硫酸工业环境保护复习重点1.接触法制硫酸的生产过程和化学原理
2.保护环境难点聚焦一、接触法制硫酸的原理、过程及典型设备1.三种原料:硫铁矿( FeS2)、空气、水
利用接触法制硫酸一般可以用硫黄、黄铁矿、石膏、有色金属冶炼厂的烟气 ( 含一定量的SO2) 等
其中用硫黄作原料成本低、对环境污染少
但我国硫黄资源较少,主要用黄铁矿(主要成分为FeS2)作生产硫酸的原料
2 .三步骤、三反应:(1)4FeS2 +11O2=== 2Fe2O3+8SO2(高温)(2)2 SO2+ O2≒2 SO3(催化剂,加热),(3)SO3 + H2O === H2SO4 3.三设备:(1)沸腾炉( 2)接触室( 3)合成塔4.三原理:化学平衡原理、热交换原理、逆流原理
(1)增大反应物浓度、增大反应物间接触面积,能提高反应速率并使化学平衡向正反应方向移动,以充分提高原料利用率
(2)热交换原理:在接触室中生成的热量经过热交换器,传递给进入接触室的需要预热的混合气体, 为二氧化硫的接触氧化和三氧化硫的吸收创造了有利条件
(3)逆流原理:液体由上向下流,气体由下向上升,两者在逆流过程中充分反应
实 用 文 档2 接触法制硫酸的原理、过程及典型设备三原料三阶段三反应(均放热)三设备三净化黄铁矿或 S 造气4FeS2+11O2== 2Fe2O3+8SO2(高温)或 S+O2=SO2 沸腾炉除尘空气接触氧化2 SO2 + O2≒2 SO3(催化剂)接触室(含热交换器)洗涤98
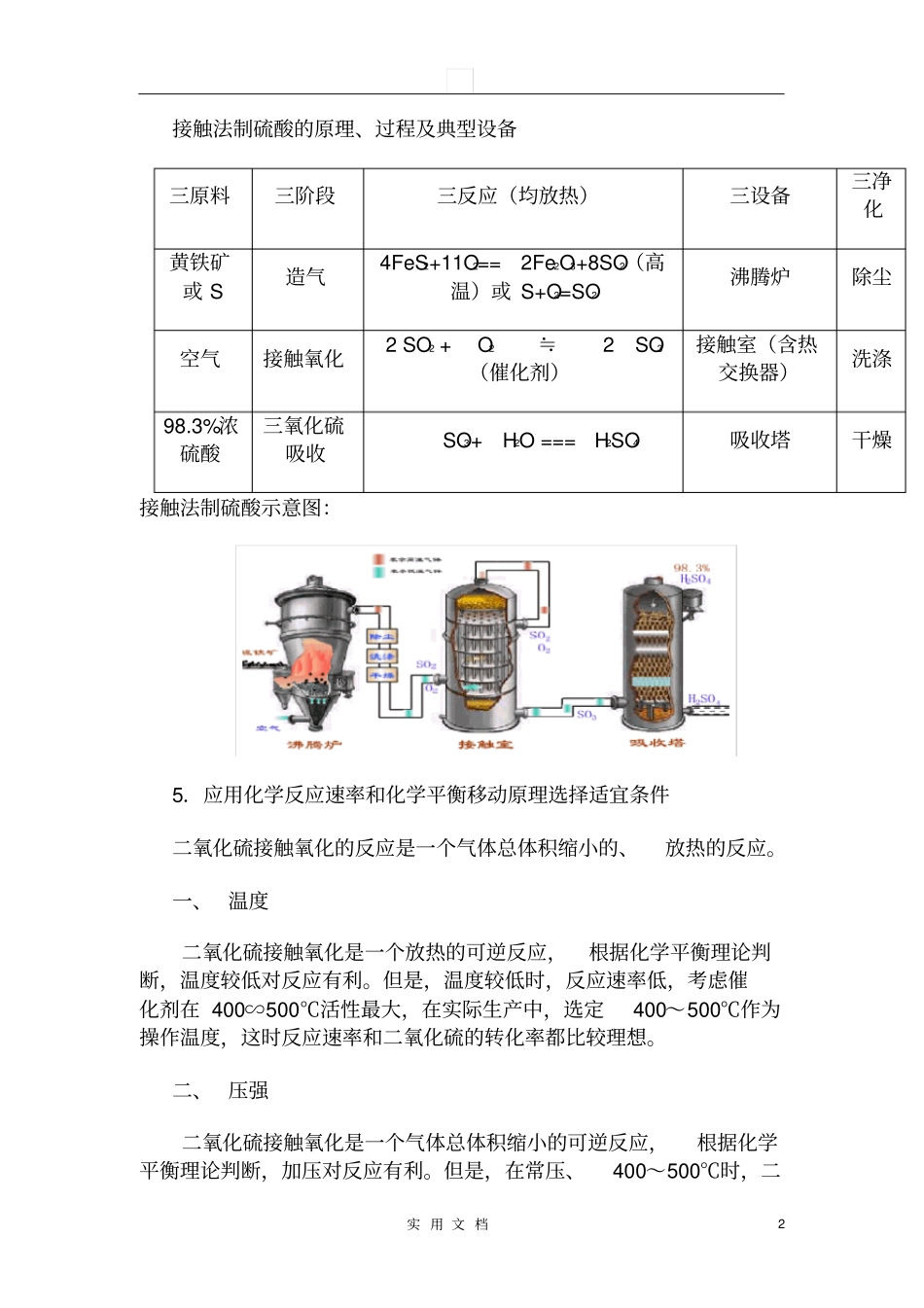
3%浓硫酸三氧化硫吸收SO3+ H2O === H2SO4 吸收塔干燥接触法制硫酸示意图:5.应用化学反应速率和化学平衡移动原理选择适宜条件二氧化硫接触氧化的反应是一个气体总体积缩小的、放热的反应
一、 温度二氧化硫接触氧化是一个放热的可逆反应,根据化学平衡理论判断,温度较低对反应有利
但是,温度较低时,反应