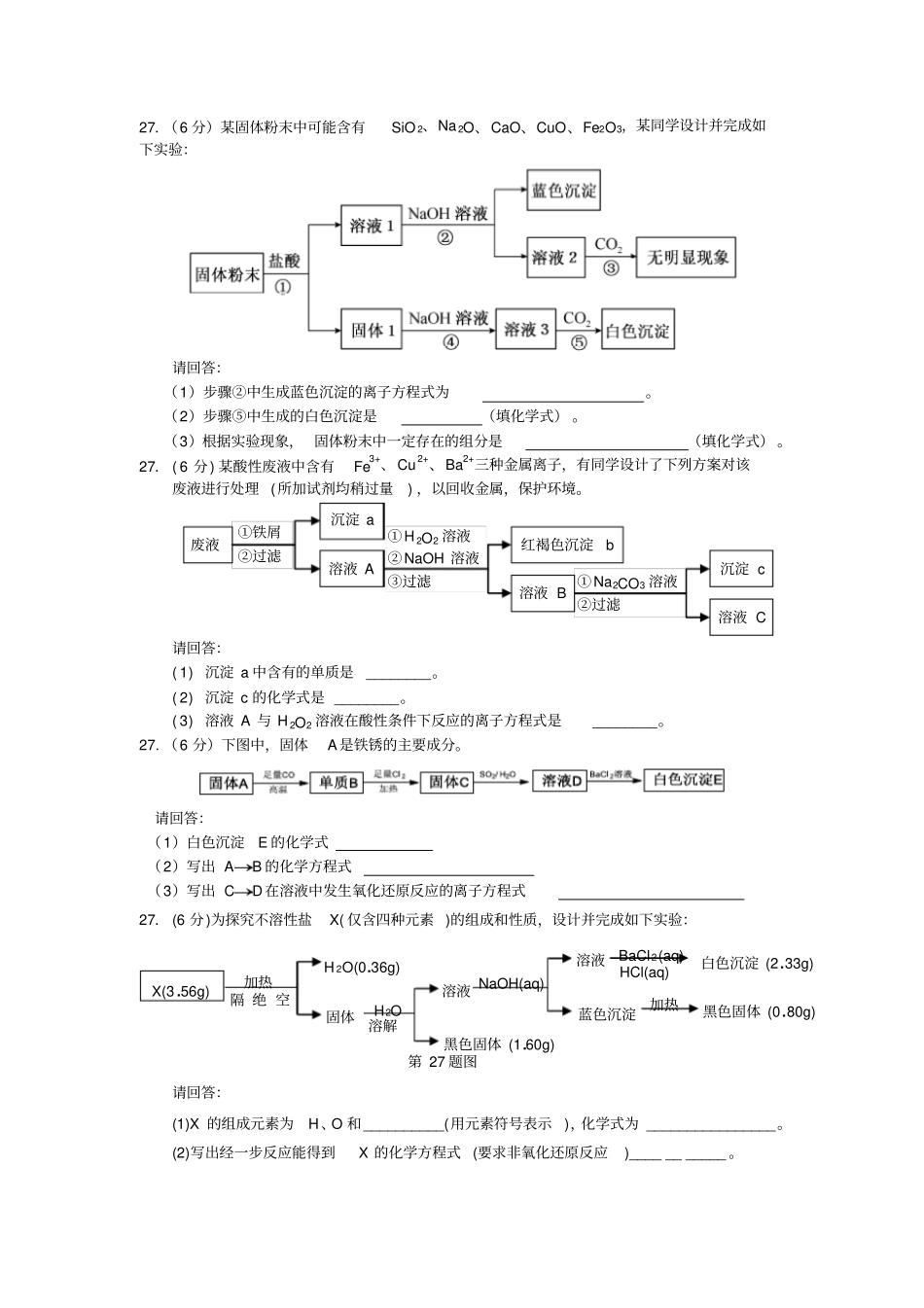
27.(6 分)某固体粉末中可能含有SiO 2、Na 2O、CaO、CuO、Fe2O3,某同学设计并完成如下实验:请回答:(1)步骤②中生成蓝色沉淀的离子方程式为
(2)步骤⑤中生成的白色沉淀是(填化学式)
(3)根据实验现象, 固体粉末中一定存在的组分是(填化学式)
27. ( 6 分) 某酸性废液中含有Fe3+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对该废液进行处理 (所加试剂均稍过量) ,以回收金属,保护环境
请回答:( 1) 沉淀 a 中含有的单质是________
( 2) 沉淀 c 的化学式是 ________
( 3) 溶液 A 与 H 2O2 溶液在酸性条件下反应的离子方程式是________
(6 分)下图中,固体A是铁锈的主要成分
请回答:(1)白色沉淀E 的化学式(2)写出 AB 的化学方程式(3)写出 CD在溶液中发生氧化还原反应的离子方程式27. (6 分)为探究不溶性盐X( 仅含四种元素 )的组成和性质,设计并完成如下实验:请回答:(1)X 的组成元素为H、O 和__________(用元素符号表示),化学式为 ________________
(2)写出经一步反应能得到X 的化学方程式 (要求非氧化还原反应)____ __ _____
56g) 隔 绝 空加热H 2O(0
36g) 固体溶解H2O 溶液黑色固体 (1
60g) 溶液蓝色沉淀黑色固体 (0
80g) BaCl2(aq) NaOH(aq) HCl(aq) 加热白色沉淀 (2
33g) 第 27 题图①Na2CO3 溶液②过滤①H 2O2 溶液②NaOH 溶液③过滤①铁屑②过滤废液溶液 A 沉淀 a 溶液 B 红褐色沉淀b 溶液 C 沉淀 c 27. (4 分)单质硅由于其成熟的生产工艺,丰富的生产原料及优异的性能被广泛用于电子行业及太阳能电池的