3分子轨道理论和分子轨道理论和双原子分子结构双原子分子结构3
1简单分子轨道理论1分子轨道的概念与原子类似,对分子仍采用单电子近似:电子在整个分子形成的有效势中运动,分子的空间波函数是每个电子的空间波函数的乘积:NiiiiiNNNNNNNzyxzyxzyxzyxzyxzyx122221111111),,(),,(),,(),,(),,,,,,(单电子波函数就是分子轨道2分子轨道的形成(1)在单电子近似下的分子轨道(即单电子空间波函数),可以由原子轨道的线性组合构成
(2)分子轨道的个数等于构成它的原子轨道的个数,轨道个数不变,但轨道能级改变,分子轨道能级低于原子轨道能级的称为成键轨道,反之为反键轨道
例:对于甲烷分子来说,其分子轨道可以用四个氢原子的1s轨道以及碳原子的1s,2s,2px,2py和2pz线性叠加构成
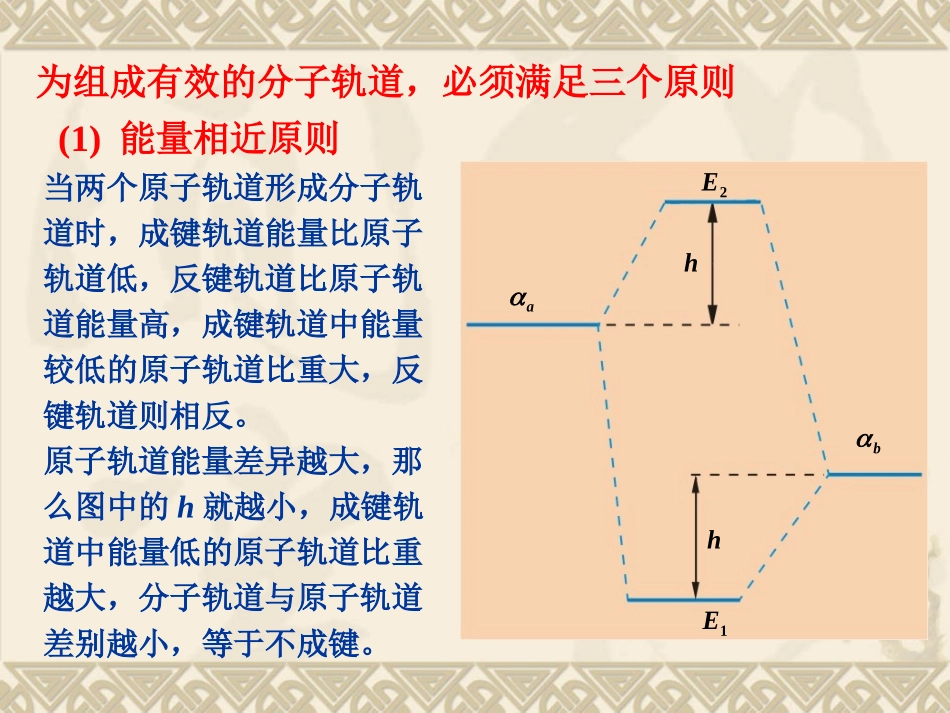
(3)分子轨道相互正交——线性组合不是随意的为组成有效的分子轨道,必须满足三个原则(1)能量相近原则2E1Eabhh当两个原子轨道形成分子轨道时,成键轨道能量比原子轨道低,反键轨道比原子轨道能量高,成键轨道中能量较低的原子轨道比重大,反键轨道则相反
原子轨道能量差异越大,那么图中的h就越小,成键轨道中能量低的原子轨道比重越大,分子轨道与原子轨道差别越小,等于不成键
(2)轨道最大重叠原则:成键的方向性
(3)对称性匹配原则:最重要的一条原则,决定是否能够成键,其他原则只影响成键效率
如图,s轨道和p轨道重叠,由于对称性不匹配,p轨道上下符号相异,重叠的结果等于零
3关于反键轨道(1)反键轨道是整个分子轨道不可或缺的组成部分,几乎占总分子轨道数的一半
(2)反键轨道与成键轨道性质相似,也必须按照Pauli不相容原理、能量最低原理和Hund规则填充电子
(3)反键轨道并不是总处于排斥的状态
(4)反键轨道是了解分子激发态性质的