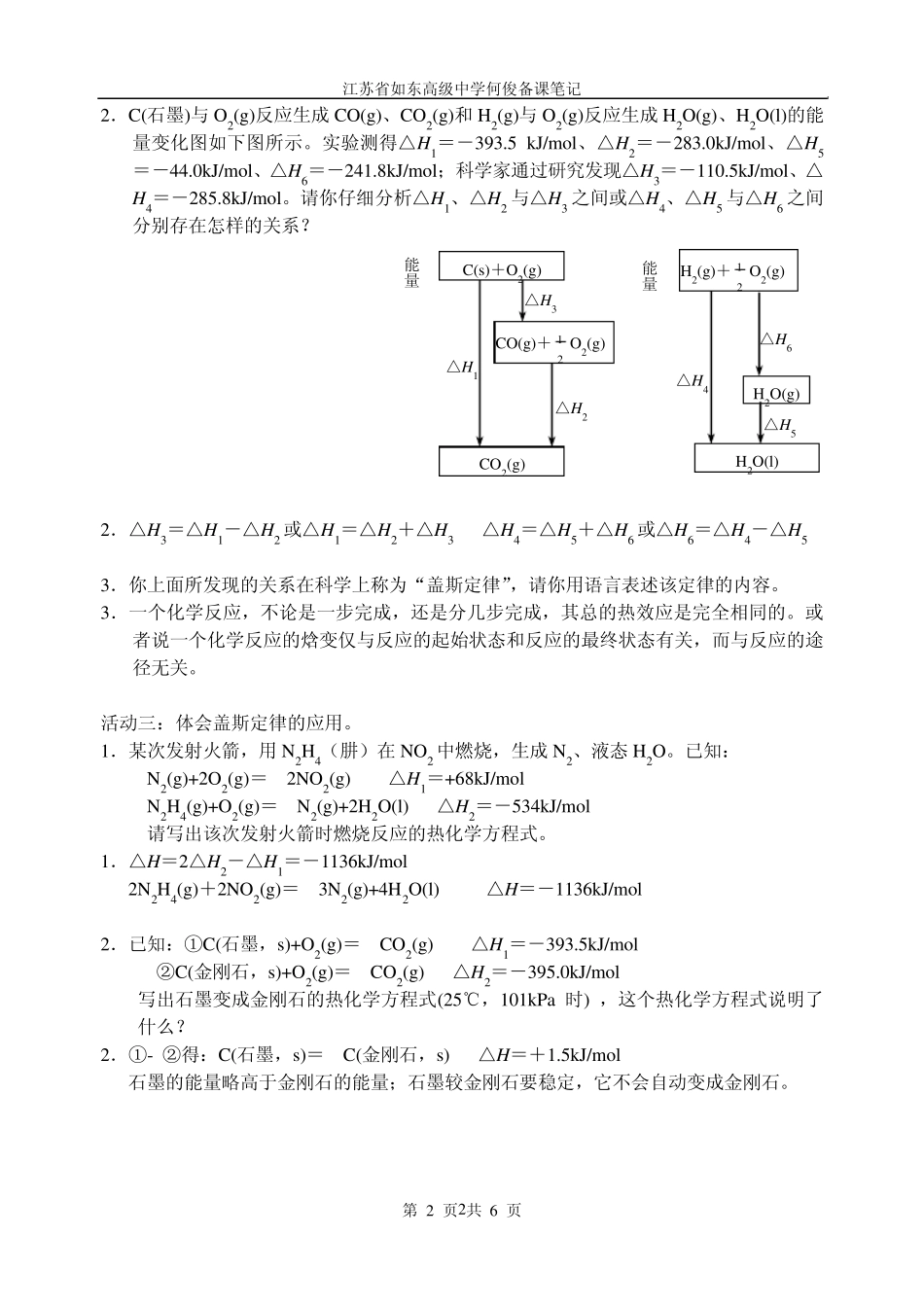
江苏省如东高级中学何俊备课笔记 第 1 页 共 6 页 1 第三节 化学反应热的计算 【学习目标】1.学会有关反应热的简单计算。 2.认识并简单应用盖斯定律。 【活动过程】 活动一:学会有关反应热的简单计算。 1.25℃、101kPa 下,碳、氢气、甲烷和葡萄糖的燃烧热依次是 393.5kJ/mol、285.8kJ/mol、890.3kJ/mol、2800kJ/mol,则下列热化学方程式中正确的有哪些? ⑴C(s)+21 O2(g)=CO(g) △H=-393.5 kJ/mol ⑵2H2(g)+O2(g)=2H2O(g) △H=+571.6 kJ/mol ⑶CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3 kJ/mol ⑷21 C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l) △H=-1400 kJ/mol 1.⑷ 2.人们把在 298K、101kPa 条件下,1 mol AB 气态分子生成气态 A 原子和 B 原子的过程中所吸收的能量,称为 AB 间共价键的键能。已知 H-H 的键能为 436 kJ/mol,H-N的键能为 391 kJ/mol。根据热化学方程式 N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ/mol,则 N≡N 的键能是多少? 2.945.6 kJ/mol 3.298K、101kPa 时,将 1.0 g 钠与足量的氯气反应,生成氯化钠晶体并放出 17.87 kJ 的热量,求生成 1mol 氯化钠的反应热? 3.411.01kJ/mol 4.已知:C(s)+O2(g)=CO2(g) △H=-393.5 kJ/mol CaCO3(s)=CaO(s)+CO2(g) △H=+178.2 kJ/mol 若要将 1 t 碳酸钙煅烧成生石灰,理论上需用多少千克焦炭? 4.54.34kg 活动二:认识并理解盖斯定律。 1.某人要从山下的A 点到达山顶 B 点,他从 A 点出发,可以历经不同的途径和不同的方式。你认为他有哪些可能的途径或方式?当他到达 B 点后所发生的势能变化是否相同? 1.翻山越岭攀登而上或拾级蜿蜒而上或乘坐索道缆车直奔山顶 势能变化相同 高温、高压 催化剂 江苏省如东高级中学何俊备课笔记 第 2 页 共 6 页 2 2.C(石墨)与O2(g)反应生成CO(g)、CO2(g)和H2(g)与O2(g)反应生成H2O(g)、H2O(l)的能量变化图如下图所示。实验测得△H1=-393.5 kJ/mol、△H2=-283.0kJ/mol、△H5=-44.0kJ/mol、△H6=-241.8kJ/mol;科学家通过研究发现△H3=-110.5kJ/mol、△H4=-285.8kJ/mol。请你仔细分析△H1、△H2 与△H3 之间或△H4、△H5 与△H6 之间分别存在怎样的关系? 2.△H3=△H1-△H2 或△H1=△H2+△H3 △H4=△H5+△H6 或△H6=△H4-△H5 3.你上面所发现的关系在科学上称为“盖斯定律”,请...