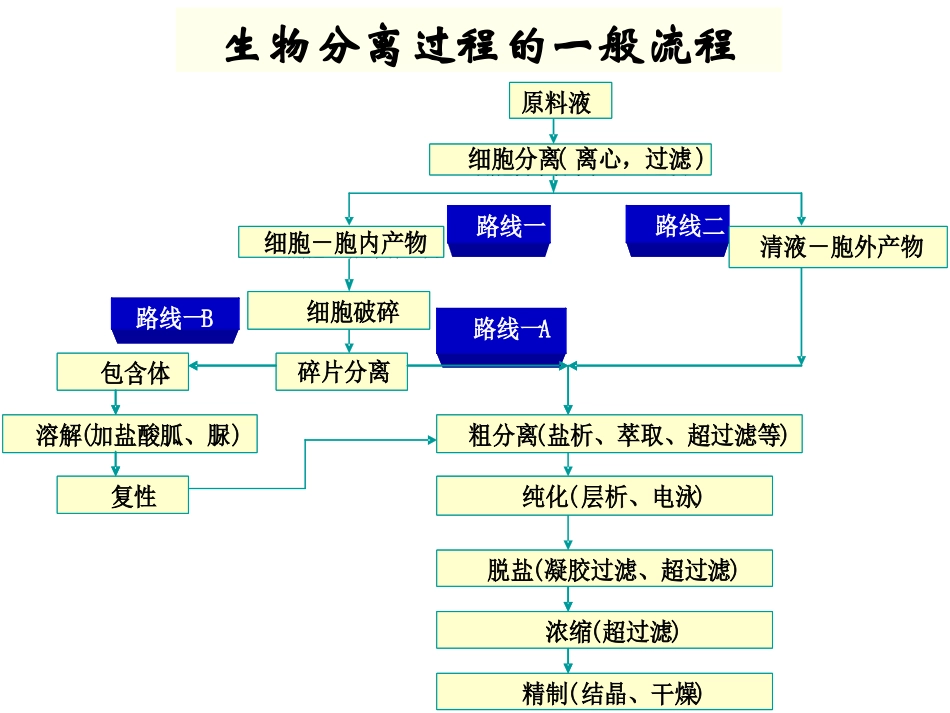
第五章沉淀分离5.1概述5.2盐析法5.3有机溶剂沉淀法5.4非离子多聚物沉淀法5.5其他沉淀法生物分离过程的一般流程原料液细胞分离(离心,过滤)细胞-胞内产物路线一路线二细胞破碎碎片分离路线一A路线一B清液-胞外产物粗分离(盐析、萃取、超过滤等)纯化(层析、电泳)脱盐(凝胶过滤、超过滤)浓缩(超过滤)精制(结晶、干燥)包含体溶解(加盐酸胍、脲)复性原料液细胞分离(离心,过滤)细胞-胞内产物路线一路线二细胞破碎碎片分离路线一A路线一B清液-胞外产物粗分离(盐析、萃取、超过滤等)纯化(层析、电泳)脱盐(凝胶过滤、超过滤)浓缩(超过滤)精制(结晶、干燥)包含体溶解(加盐酸胍、脲)复性5.1概述•沉淀的概念沉淀是溶液中的溶质由液相变成固相的过程。在生物工业、有机化工工业、无机化工工业及实验室分析中,沉淀都是分离与纯化中最常用的方法之一。沉淀:溶质→固相5.1概述•沉淀的作用有二:一是浓缩,通过沉淀目的产物由液相变成固相,浓缩倍数可达几十倍至数百倍;二是纯化,通过沉淀固液分相后,除去留在液相(如果目的产物是固相)或沉积在固相中(目的产物留在液相)的杂质。沉淀法操作步骤:①首先加入沉淀剂,②沉淀剂的陈化,促进粒子生长;③离心或过滤,收集沉淀物。加沉淀剂的方式和陈化条件对产物的纯度、收率和沉淀物的形状都有很大影响。5.1概述•沉淀分离的应用沉淀分离具有成本低、收率高、浓缩倍数大和操作简单等优点,因而广泛应用于氨基酸、酶制剂、抗菌素等生物工业中。对于某些不需纯度要求的生物产品(如工业用酶制剂),沉淀分离是一种常用提取方法。但对于某些纯度要求很高的生物产品,在沉淀分离中,浓缩作用常大于纯化作用,因而沉淀分离通常作为初步分离的一种方法。5.1概述•沉淀剂的选择沉淀剂的作用是降低溶质的溶解度使之析出,除考虑沉淀效果外还需考虑下列因素:(1)沉淀剂对目的产物的结构与活性是否有破坏作用;(2)沉淀剂是否容易除去(离子交换、蒸发、萃取等);(3)沉淀剂是否有毒性。5.1概述•沉淀的分类:沉淀法有许多种,根据所用沉淀剂的不同,生物工业中常用的沉淀方法有如下几种:①盐析法:多用于蛋白质和酶的分离纯化。②有机溶剂法:多用于生物小分子、多糖及核酸类产品的分离与纯化,有时也用于蛋白质和酶的沉淀。③等电点沉淀法:用于氨基酸、蛋白质等两性物质的沉淀,但此法单独应用较少,多与其它方法结合使用。5.1概述④非离子型聚合物沉淀法:用于生物大分子,是发展很快的一种方法。⑤生成盐类复合物沉淀法:用于多种化合物(其中主要是酸性或碱性化合物),其中小分子物质的沉淀应用较多。⑥选择变性沉淀法:热变性或酸碱变性沉淀法,常用于除去某些不耐热及在一定pH值下易变性的杂蛋白。但应以在实验条件下所分离物质的活性不受影响为前提。5.2盐析法一般说来,所有固性溶质都可以在溶液中加入中性盐而沉淀析出,这一过程称为盐析。盐析法具有如下特点:(1)成本低,不需要什么特别昂贵的设备;(2)操作简单、安全;(3)对许多生物活性物质具有稳定作用;(4)存在产品与杂质的共沉作用,因而它只能作为初步纯化。5.2.1基本原理5.2.1.1盐析原理•蛋白分子的表面同时含有带电荷的亲水基团和不带电荷的疏水基团。•蛋白质的溶解度差别——取决于蛋白质分子中极性基团与非极性基团的比例和这些基团的排列位置。5.2.1.1盐析原理(1)水合作用:•在水溶液中,蛋白质分子中的亲水基团吸聚着许多水分子,这种作用称为水合作用。这些水分子在蛋白质分子的表面形成一层水化膜。•由于水膜的存在,各蛋白质分子间彼此隔开,使蛋白质分子在水中呈溶解状态。稳定的亲水溶液分子间彼此隔开形成水化膜水分子亲水基团水合作用5.2.1.1盐析原理(2)盐溶作用(Salt-in):•蛋白质在低盐浓度下发生盐溶,这是因为当向蛋白质溶液中加入少量中性盐时,中性盐离子对蛋白质分子表面亲水基团(及水活度)的影响,增强了蛋白质分子与水分子的相互作用力,从而使蛋白质的溶解度增大。蛋白质溶液少量中性盐增加蛋白质分子与水分子的相互作用→蛋白质溶解度↑5.2.1.1盐析原理•蛋白质在高盐浓度下发生盐析,这是因为当中性盐...