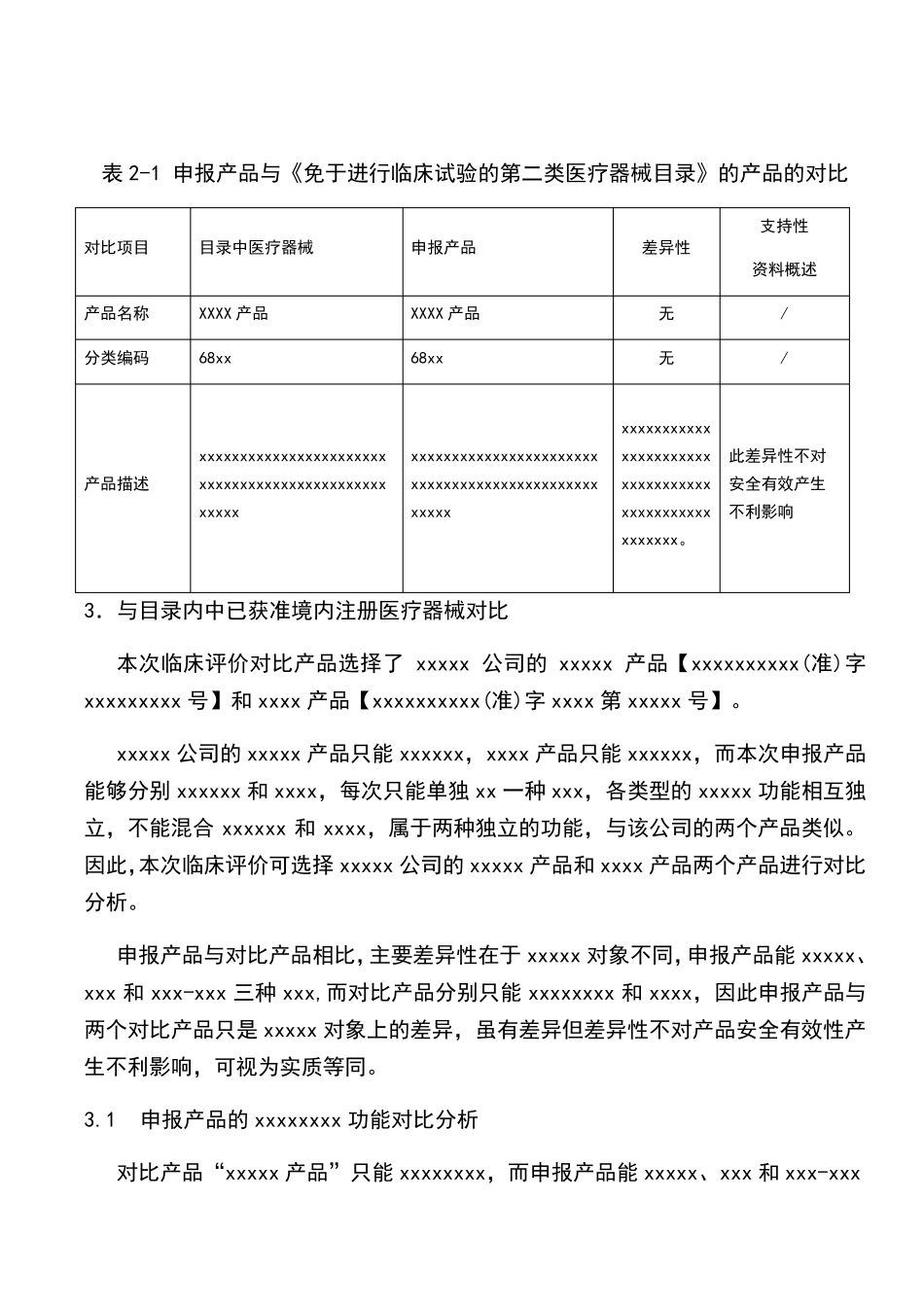
XXXX 产 品 临床评价报告 文件编号 XXX-XXX-01 修订版次 XXX 产品名称 XXXX 产品 是否受控 否 编 制 XXX 日 期 2016 年 3 月 5 日 审 核 XXX 日 期 2016 年 3 月 5 日 批 准 XXX 日 期 2016 年 4 月 19 日 编制单位 XXXXX 公司 XXXX 产品临床评价报告 1.临床评价概述 申报产品XXXX 产品已在国内外应用多年,是较为成熟、使用广泛的临床医疗器械产品。 本次申报产品与《免于进行临床试验的第二类医疗器械目录》中第 xxx 个分类编码 68xx 中的 XXXX 产品的描述相同,属于免于临床试验的产品,详见本报告第二部分:2.与临床豁免目录内中的产品描述对比 本次申报产品与目录内中已获准境内注册医疗器械对比产品选取了 xxxxx 公司的 xxxxx 产品【xxxxxxxxxx(准)字 xxxxxxxxx 号】和 xxxx 产品【xxxxxxxxxx(准)字 xxxx 第 xxxxx 号】,该企业的 xxxxx 产品产品只能 xxxxxx,其 xxxx 产品只能xxxxxx。本次申报产品能够分别 xxxxxx 和 xxxx,但不能同时或交叉 xxxxxx 和 xxxx,因此可与 xxxxx 产品、xxxx 产品两个产品进行对比。通过对比分析得出结论,申报产品的作用原理、组成结构和适用范围与对比产品基本相同,申报产品与目录中的产品虽有差异,但差异性不对产品安全有效性产生不利影响,可视为实质等同。(对比产品注册证信息(附件3)来源于国家食品药品监督管理总局的医疗器械数据查询系统以及对比产品的说明书 (附件4)) 2. 与临床豁免目录内中的产品描述对比 本次申报产品XXXX 产品属于医疗器械分类目录 68xx 产品-4 xxxxx 产品产品,与《免于进行临床试验的第二类医疗器械目录》中的 XXXX 产品产品描述一 致 ,详见申报产品与表 2-1《免于进行临床试验的第二类医疗器械目录》的产品对比: 表2-1 申报产品与《免于进行临床试验的第二类医疗器械目录》的产品的对比 对比项目 目录中医疗器械 申报产品 差异性 支持性 资料概述 产品名称 XXXX 产品 XXXX 产品 无 / 分类编码 68xx 68xx 无 / 产品描述 xxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxx xxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxx xxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxxx。 此差异性不对安全有效产生不利影响 3.与目录内中已获准境内注册医疗器械对比 本次临床评价对比产品选择了xxxxx 公司的xxxxx 产品【xxxxxx...