厂房与设施验证方案文件编号:江西隆莱生物制药有限公司1
验证方案的起草与审批1
1 验证方案的起草1
2 验证方案的审批2
验证机构与人员职责3
实施计划与程序5
相关文件与标准依据6
验证目的与范围7
1 厂房与设施的预确认7
2 厂房与设施的安装确认7
3 厂房与设施的运行确认7
4 厂房与设施的性能确认8
1 再验证8
2 验证周期9
附录1 验证方案的起草与审批1
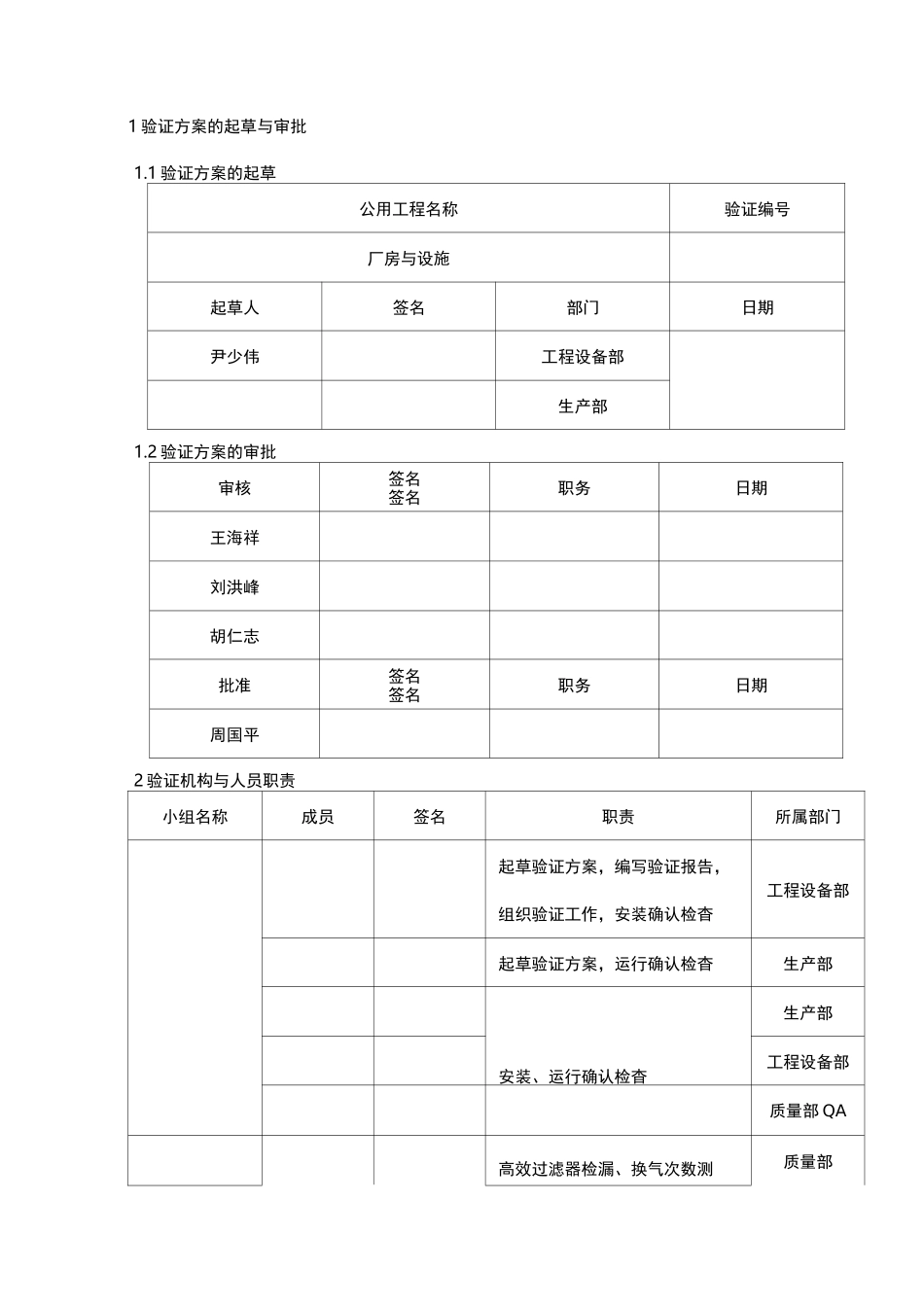
1 验证方案的起草公用工程名称验证编号厂房与设施起草人签名部门日期尹少伟工程设备部生产部1
2 验证方案的审批审核签名签名职务日期王海祥刘洪峰胡仁志批准签名签名职务日期周国平2 验证机构与人员职责小组名称成员签名职责所属部门起草验证方案,编写验证报告,组织验证工作,安装确认检杳工程设备部起草验证方案,运行确认检杳生产部安装、运行确认检杳生产部工程设备部质量部 QA高效过滤器检漏、换气次数测质量部验证工作小组定、空气中臭氧浓度的测定、性能确认检杳质量部质量部质量部质量部3 概述江西隆莱生物制药有限公司位于工业区,四周环境良好,厂区现有 2个出入口,人流出入口靠厂区东面,物流出入口靠厂区南面
车间电缆等动力管线敷设在管道架、管道沟、技术夹层,符合 GMP 规范要求
车间位于厂区 2#楼,总面积为约 532 朮其中 317 为 10 万级洁净区
用于生产原料药的精制脱色、结晶、离心、烘干、粉碎、混合、包装等生产工艺过程
车间的设计、安装均按 GMP 要求进行
在本验证中,通过与车间生产有关的厂房与设施的预确认、安装确认、运行确认、性能确认来证明车间的厂房设施不会对生产过程造成污染,在此厂房内能生产出合格的产品
4 实施计划与程序验证总时间:日期验证开始时间验证完成时间5 相关文件与标准依据5
1 标准依据《药品生产质量管理规范》2010 版《洁净厂房设计规范》GB