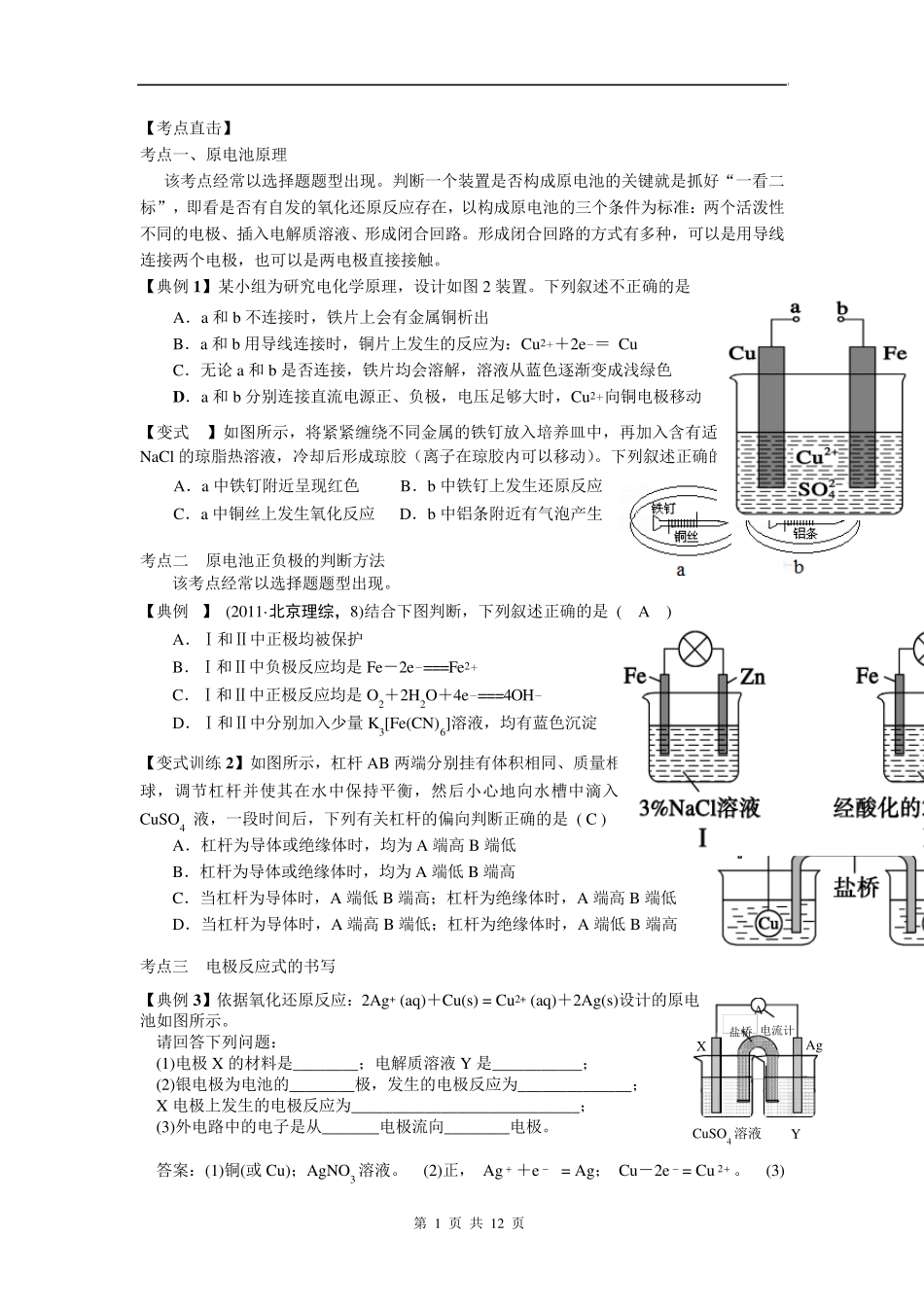
第 1 页 共 12 页 盐桥 X Y A CuSO4 溶液 电流计 Ag 【考点直击】 考点一、原电池原理 该考点经常以选择题题型出现。判断一个装置是否构成原电池的关键就是抓好“一看二标”,即看是否有自发的氧化还原反应存在,以构成原电池的三个条件为标准:两个活泼性不同的电极、插入电解质溶液、形成闭合回路。形成闭合回路的方式有多种,可以是用导线连接两个电极,也可以是两电极直接接触。 【典例 1】某小组为研究电化学原理,设计如图 2 装置。下列叙述不正确的是 A.a 和 b 不连接时,铁片上会有金属铜析出 B.a 和 b 用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu C.无论 a 和 b 是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 D .a 和 b 分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动 【变式 1】如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl 的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动)。下列叙述正确的是 ( B) A.a 中铁钉附近呈现红色 B.b 中铁钉上发生还原反应 C.a 中铜丝上发生氧化反应 D.b 中铝条附近有气泡产生 考点二 原电池正负极的判断方法 该考点经常以选择题题型出现。 【典例 2】 (2011·北京理综,8)结合下图判断,下列叙述正确的是 ( A ) A.Ⅰ和Ⅱ中正极均被保护 B.Ⅰ和Ⅱ中负极反应均是Fe-2e-===Fe2+ C.Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-===4OH- D.Ⅰ和Ⅱ中分别加入少量 K3[Fe(CN)6]溶液,均有蓝色沉淀 【变式训练 2】如图所示,杠杆 AB 两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4 液,一段时间后,下列有关杠杆的偏向判断正确的是 ( C ) A.杠杆为导体或绝缘体时,均为 A 端高 B 端低 B.杠杆为导体或绝缘体时,均为 A 端低 B 端高 C.当杠杆为导体时,A 端低 B 端高;杠杆为绝缘体时,A 端高 B 端低 D.当杠杆为导体时,A 端高 B 端低;杠杆为绝缘体时,A 端低 B 端高 考点三 电极反应式的书写 【典例 3】依据氧化还原反应:2Ag+ (aq)+Cu(s) = Cu2+ (aq)+2Ag(s)设计的原电池如图所示。 请回答下列问题: (1)电极 X 的材料是________;电解质溶液Y 是___________; (2)银电极为电池的________极,发生的电极反应为______________; X 电极上发生...