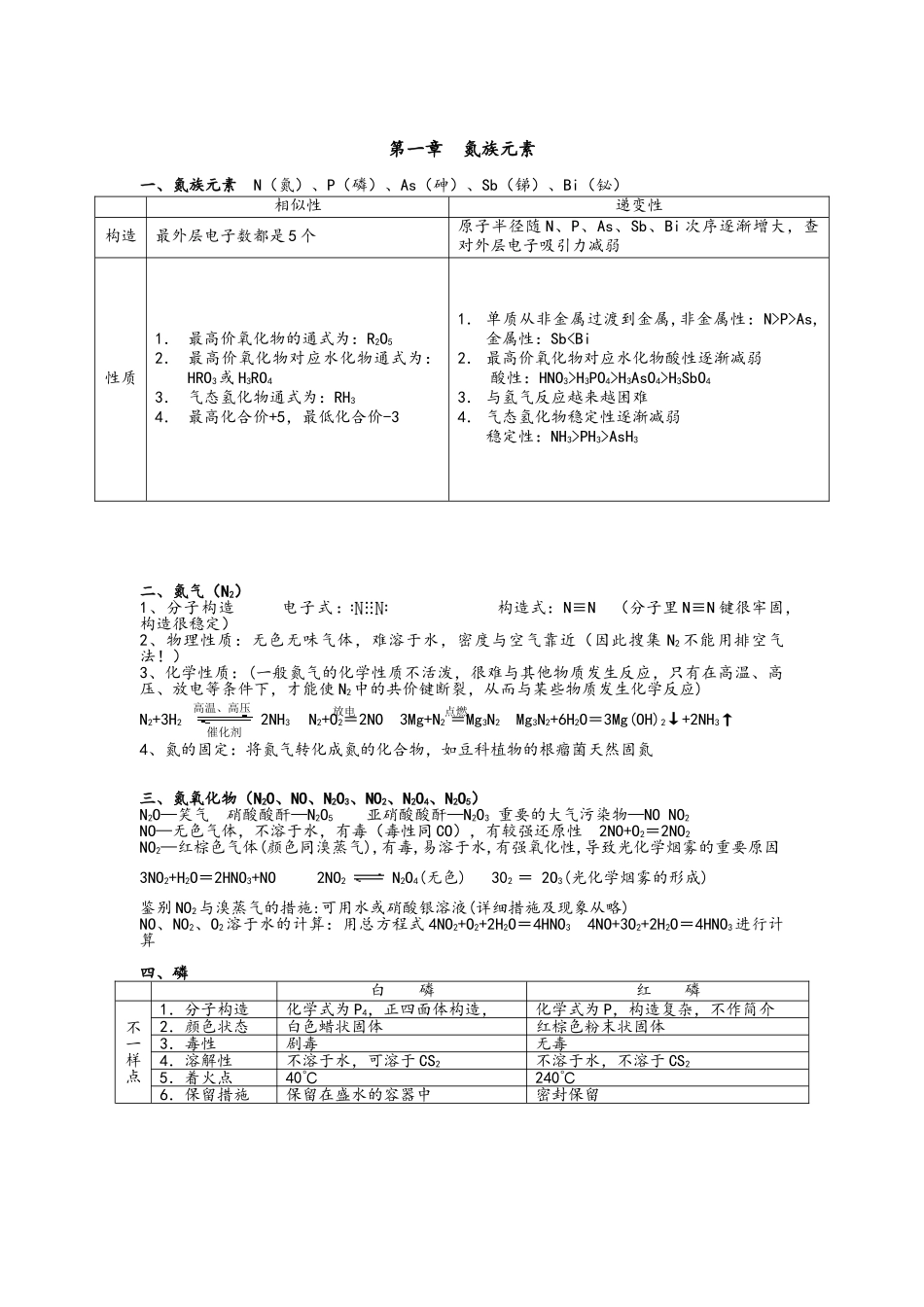
第一章 氮族元素一、氮族元素 N(氮)、P(磷)、As(砷)、Sb(锑)、Bi(铋)相似性递变性构造最外层电子数都是 5 个原子半径随 N、P、As、Sb、Bi 次序逐渐增大,查对外层电子吸引力减弱性质1. 最高价氧化物的通式为:R2O52. 最高价氧化物对应水化物通式为:HRO3或 H3RO43. 气态氢化物通式为:RH34. 最高化合价+5,最低化合价-31. 单质从非金属过渡到金属,非金属性:N>P>As,金属性:SbH3PO4>H3AsO4>H3SbO43. 与氢气反应越来越困难4. 气态氢化物稳定性逐渐减弱稳定性:NH3>PH3>AsH3二、氮气(N2)1、分子构造 电子式: 构造式:N≡N (分子里 N≡N 键很牢固,构造很稳定)2、物理性质:无色无味气体,难溶于水,密度与空气靠近(因此搜集 N2 不能用排空气法
)3、化学性质:(一般氮气的化学性质不活泼,很难与其他物质发生反应,只有在高温、高压、放电等条件下,才能使 N2中的共价键断裂,从而与某些物质发生化学反应)N2+3H2 2NH3 N2+O2=2NO 3Mg+N2 =Mg3N2 Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑4、氮的固定:将氮气转化成氮的化合物,如豆科植物的根瘤菌天然固氮三、氮氧化物(N2O、NO、N2O3、NO2、N2O4、N2O5)N2O—笑气 硝酸酸酐—N2O5 亚硝酸酸酐—N2O3 重要的大气污染物—NO NO2NO—无色气体,不溶于水,有毒(毒性同 CO),有较强还原性 2NO+O2=2NO2NO2—红棕色气体(颜色同溴蒸气),有毒,易溶于水,有强氧化性,导致光化学烟雾的重要原因3NO2+H2O=2HNO3+NO 2NO2 N2O4(无色) 302 = 2O3(光化学烟雾的形成)鉴别 NO2与溴蒸气的措施:可用水或硝酸银溶液(详细措施及现象从略)NO、NO2、O2溶于水的