必考(21~25)拉分专练(五)选择题(本题共 5 题,每题 2 分,共 10 分)1
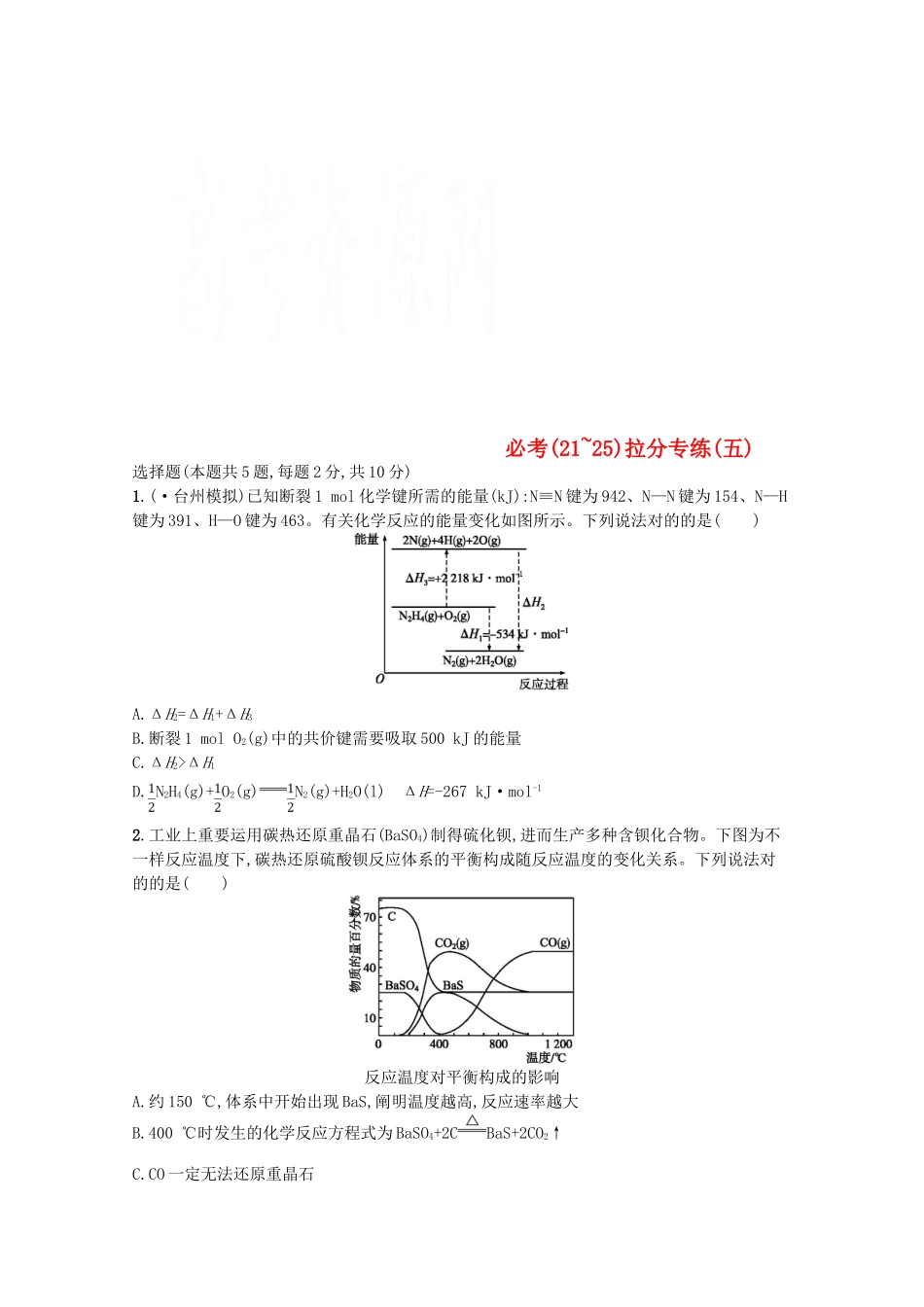
(·台州模拟)已知断裂 1 mol 化学键所需的能量(kJ):N≡N 键为 942、N—N 键为 154、N—H键为 391、H—O 键为 463
有关化学反应的能量变化如图所示
下列说法对的的是( )A
ΔH2=ΔH1+ΔH3B
断裂 1 mol O2(g)中的共价键需要吸取 500 kJ 的能量C
ΔH2>ΔH1D
N2H4(g)+ O2(g)N2(g)+H2O(l) ΔH=-267 kJ·mol-12
工业上重要运用碳热还原重晶石(BaSO4)制得硫化钡,进而生产多种含钡化合物
下图为不一样反应温度下,碳热还原硫酸钡反应体系的平衡构成随反应温度的变化关系
下列说法对的的是( )反应温度对平衡构成的影响A
约 150 ℃,体系中开始出现 BaS,阐明温度越高,反应速率越大B
400 ℃时发生的化学反应方程式为 BaSO4+2CBaS+2CO2↑C
CO 一定无法还原重晶石D
温度高于 400 ℃后,硫酸钡才能转化为 BaS3
常温下,向 20
00 mL 0
100 0 mol·L-1的醋酸溶液中逐滴加入 0
100 0 mol·L-1 NaOH 溶液,pH 随 NaOH 溶液体积的变化如图所示
下列说法不对的的是( )A
在反应过程中,c(Na+)+c(H+)=c(CH3COO-)+c(OH-)B
pH=5 时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-)C
pH=6 时,c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0
100 0 mol·L-1D
pH=7 时,消耗 NaOH 溶液的体积不不小于 20
00 mL4
(·浙江十校联盟统考)锶(Sr)为第 5 周期Ⅱ A 族元素,其化合物六水氯化锶(SrCl2·6H2O)是试验室重要的分析试剂,工