北京市医疗器械经营企业检查验收标准》总则:一、根据《医疗器械监督管理条例》和《医疗器械经营企业许可证管理办法》制定本标准
二、北京市行政区域内《医疗器械经营企业许可证》的核发、换证、变更和监督管理工作适用于本标准
三、本标准根据《医疗器械分类目录》(国药监械[2002]302 号),结合北京市医疗器械经营企业实际情况,将医疗器械产品划分以下类别:A 类:III-6846 植入材料和人工器官、III-6877 介入器材;B 类:III-6821 医用电子仪器设备、III-6822 医用光学器具、仪器及内窥镜设备、III-6845 体外循环及血液处理设备、III-6854 手术室、急救室、诊疗室设备及器具;C 类:III-6815 注射穿刺器械、111-6863 口腔科材料、111-6864 医用卫生材料及敷料、III-6865 医用缝合材料及粘合剂、III-6866 医用高分子材料及制品;D 类:III-6822 医用光学器具、仪器及内窥镜设备(软性、硬性角膜接触镜及护理用液);E 类:11-6846 植入材料和人工器官(助听器);F 类:除上述类外的其它类代号医疗器械
四、经营医疗器械的门店及药品零售企业申请“III-6815 注射穿刺器械、III-6866 医用高分子材料及制品”经营范围的按本标准 F 类专用部分要求验收
申请“III-6822 医用光学器具、仪器及内窥镜设备”经营范围的非验配类企业按 B 类专用部分要求验收;申请“11-6846 植入材料和人工器官”经营范围的非验配类企业按 F类专用部分要求验收
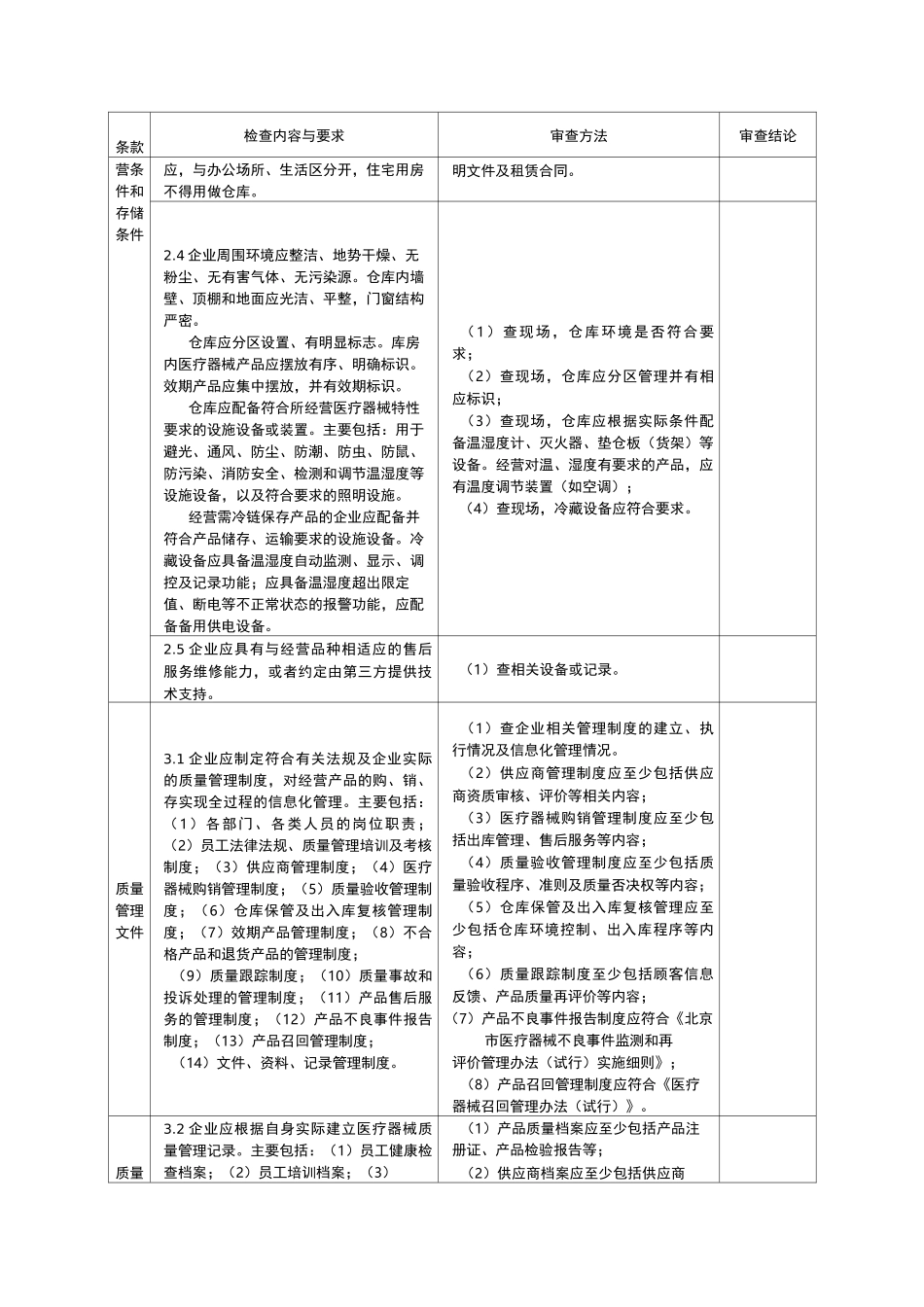
五、本标准分为通用部分和专用部分,企业应符合本标准通用部分要求和申请特定经营范围所涉及的专用部分要求
检查验收时,现场验收结果全部符合本标准的,评定为验收合格,有不符合本标准的,评定为验收不合格
六、经营体外诊断试剂及国家食品药品监督管理局另有规定的医疗器械产品