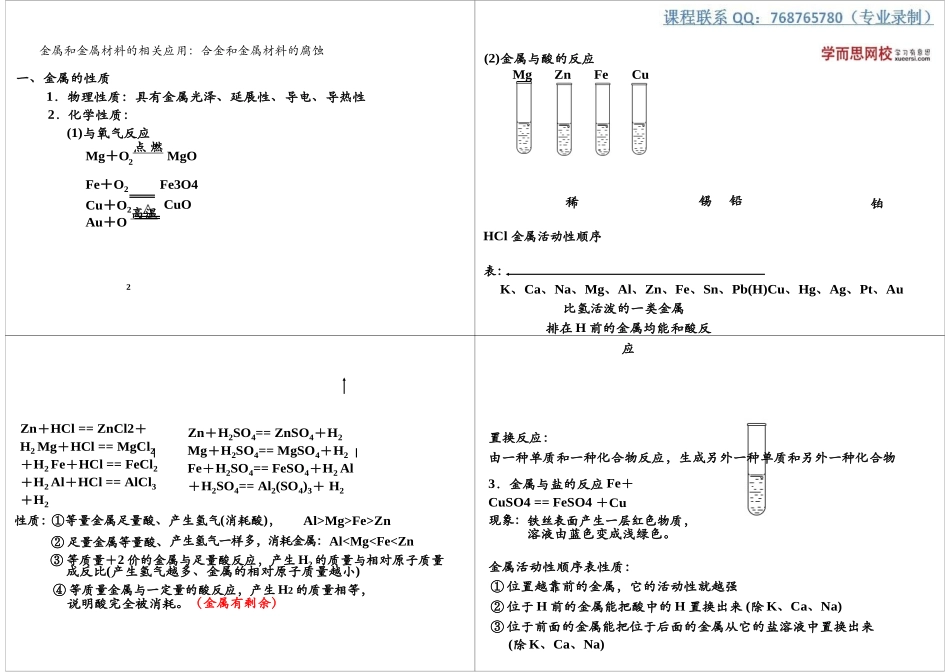
2金属和金属材料的相关应用:合金和金属材料的腐蚀一、金属的性质1.物理性质:具有金属光泽、延展性、导电、导热性2.化学性质:(1)与氧气反应Mg+O 点 燃 MgOFe+O2Fe3O4Cu+O2CuOAu+O 高温(2)金属与酸的反应MgZnFeCu稀HCl 金属活动性顺序表:锡铅铂2K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb(H)Cu、Hg、Ag、Pt、Au比氢活泼的一类金属排在 H 前的金属均能和酸反应Zn+HCl == ZnCl2+ H2 Mg+HCl == MgCl2+H2 Fe+HCl == FeCl2+H2 Al+HCl == AlCl3+H2Zn+H2SO4== ZnSO4+H2 Mg+H2SO4== MgSO4+H2 Fe+H2SO4== FeSO4+H2 Al+H2SO4== Al2(SO4)3+ H2置换反应:由一种单质和一种化合物反应,生成另外一种单质和另外一种化合物3.金属与盐的反应 Fe+CuSO4 == FeSO4 +Cu性质:①等量金属足量酸、产生氢气(消耗酸),Al>Mg>Fe>Zn② 足量金属等量酸、产生氢气一样多,消耗金属:Al