专题十 金属元素及其化合物【学法导航】1
关于 Na 元素和 F 元素的叙述正确的是 ( ) A.原子序数 Na>F YCY B.原子半径 NaCl>F;【答案】A
下列金属冶炼的反应原理,错误的是 ( ) A.2NaCl(熔融)\s\up6(通电)2Na+Cl2↑ B.MgO+H2\s\up6(△)Mg+H2O C.Fe3O4+4CO\s\up6(高温)3Fe+4CO2 D.2HgO\s\up6(△)2Hg+O2↑【方法要领】根据金属的活泼性和金属活动性顺序表来理解掌握金属冶炼的原理和方法
按照金属元素的活动性不同,金属的冶炼方法可以有电解法、还原剂还原法、加热分解法、物理法如 Au、Pt 等的冶炼等①电解法最强的金属冶炼手段几乎适合所有金属的冶炼,但考虑经济成本主要是针对活泼性强的金属来使用 K――Al;② 热还原法主要适合中等活泼的金属,如 Zn—Cu
注意还原性的强弱和化学平衡原理的使用
如 MgO 不能用 H2还原,因为 Mg的还原性强于 H2,但是可以用 C 来还原,如.MgO+C = Mg+CO 反应条件是高温,此时产物 Mg和 CO 均是气体
③热分解法适合于不活泼的金属如 Ag、Hg 的冶炼、物理法如 Au、Pt 等的冶炼等【答案】B 3.(09 年海南化学·3)除去 NaHCO3溶液中混有的少量 Na2CO3可采取的方法是:A.通入二氧化碳气体B.加入氢氧化钡溶液C.加入澄清石灰水D.加入稀盐酸【方法要领】除杂方法要操作简便、效果好、不带来新的杂质、保留非杂质成份
溶液中可用这样的方法: Na2CO3 + H2O + CO2 = 2NaHCO3【答案】A4
某溶液中可能含有 Fe2+、Mg2+、Cu2+、NH4+、Al3+中的一种或几种
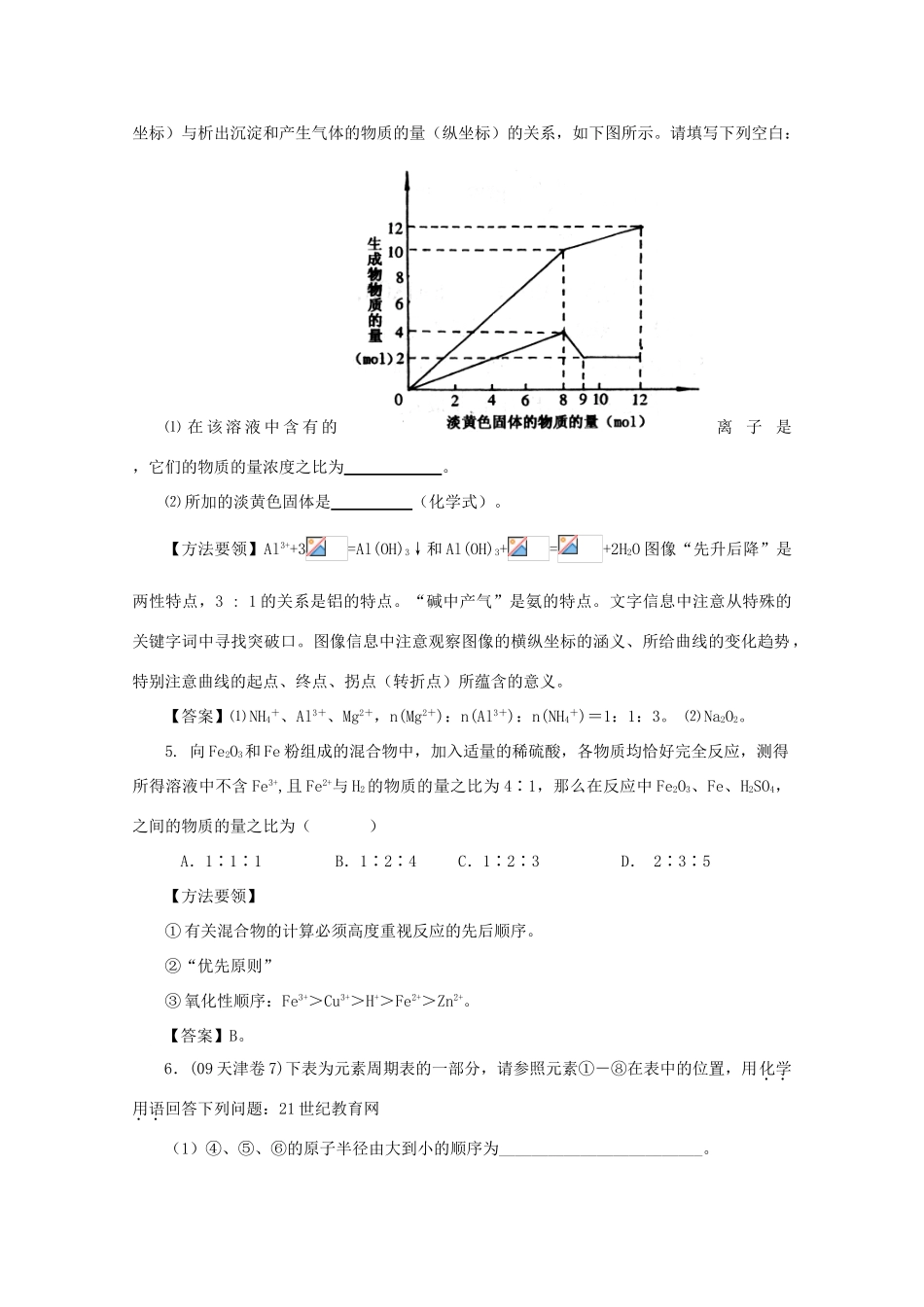
当加入一种淡黄色固体并加热溶液时,有刺激性气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出沉淀