云南省德宏州潞西市芒市中学 2014 年高中化学 化学计量在实验中的应用(第三课时)导学案 1 新人教版必修 1一、学习目标在了解气体的体积与温度和压强有密切关系的基础上,理解气体摩尔体积的概念
[思考 1]根据初中所做的电解水实验完成课本第 13 页表格,通过比较得出什么结论
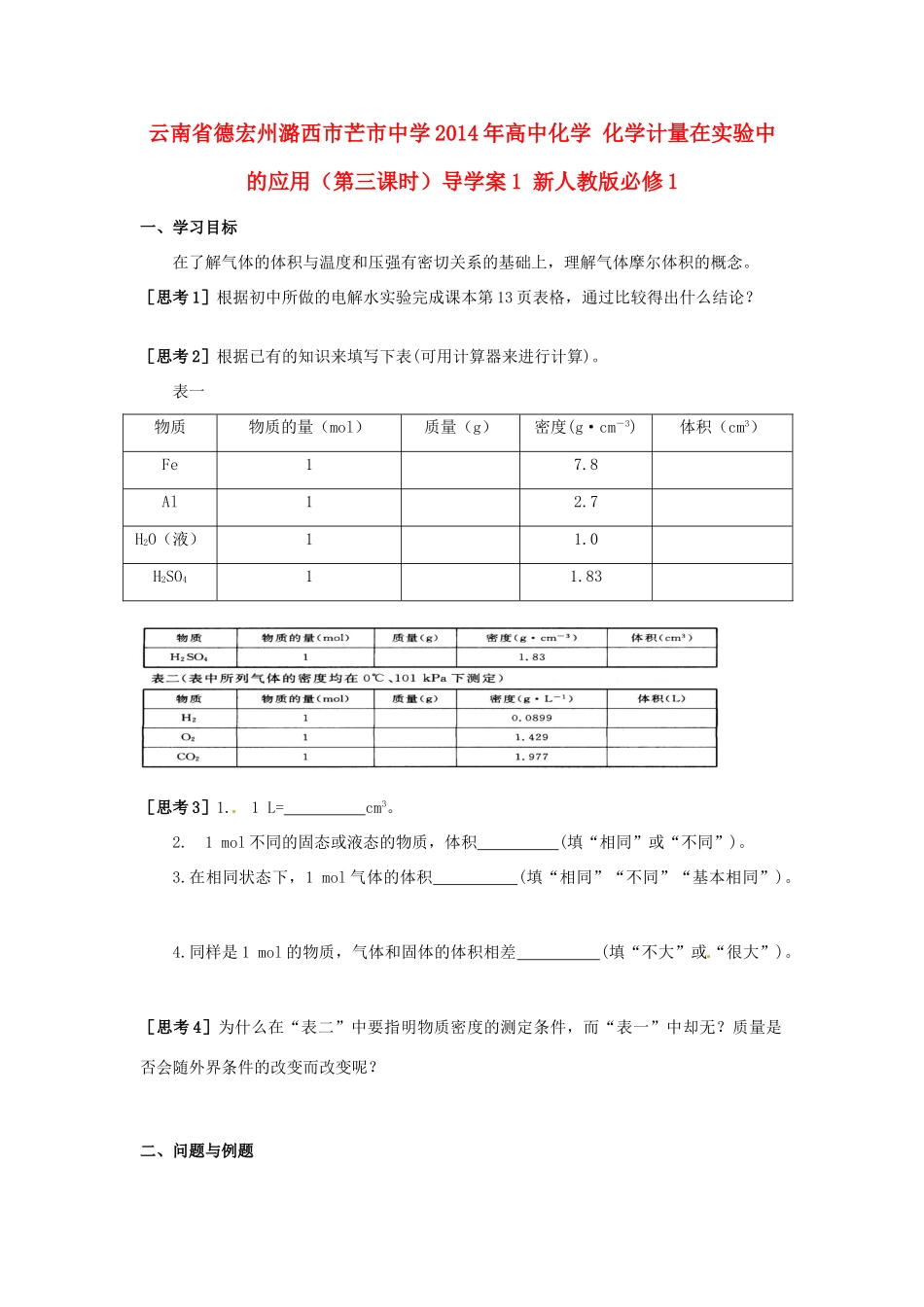
[思考 2]根据已有的知识来填写下表(可用计算器来进行计算)
表一物质物质的量(mol)质量(g)密度(g·cm-3)体积(cm3)Fe17
7H2O(液)11
0H2SO411
83[思考 3]1
1 L= cm3
1 mol 不同的固态或液态的物质,体积 (填“相同”或“不同”)
在相同状态下,1 mol 气体的体积 (填“相同”“不同”“基本相同”)
同样是 1 mol 的物质,气体和固体的体积相差 (填“不大”或 “很大”)
[思考 4]为什么在“表二”中要指明物质密度的测定条件,而“表一”中却无
质量是否会随外界条件的改变而改变呢
二、问题与例题[问题 1]物质体积的大小取决于哪些微观因素
[问题 2]当粒子数一定时,固、液、气态物质 的体积主要取决于什么因素
[问题 3]为什么相同外界条件下,1 mol 固、液态物质所具有的体积不同,而 1 mol 气态物质所具有的体积却基本相同
[问题 4]气体摩尔体积 Vm的表达式是什么
能否从气体摩尔体积 Vm的表达式中,知道其单位呢
[练习 1]判断正误,并说明理由
标况下,1 mol 任何物质的体积都约是 22
1 mol 气体的体积约为 22
标准状况下,1 mol O2和 N2混合气的体积约为 22
4 L 气体所含分子数一定大于 11
2 L 气体所含分子数
任何条件下,气体的摩尔体积都是 22
4 L/mol