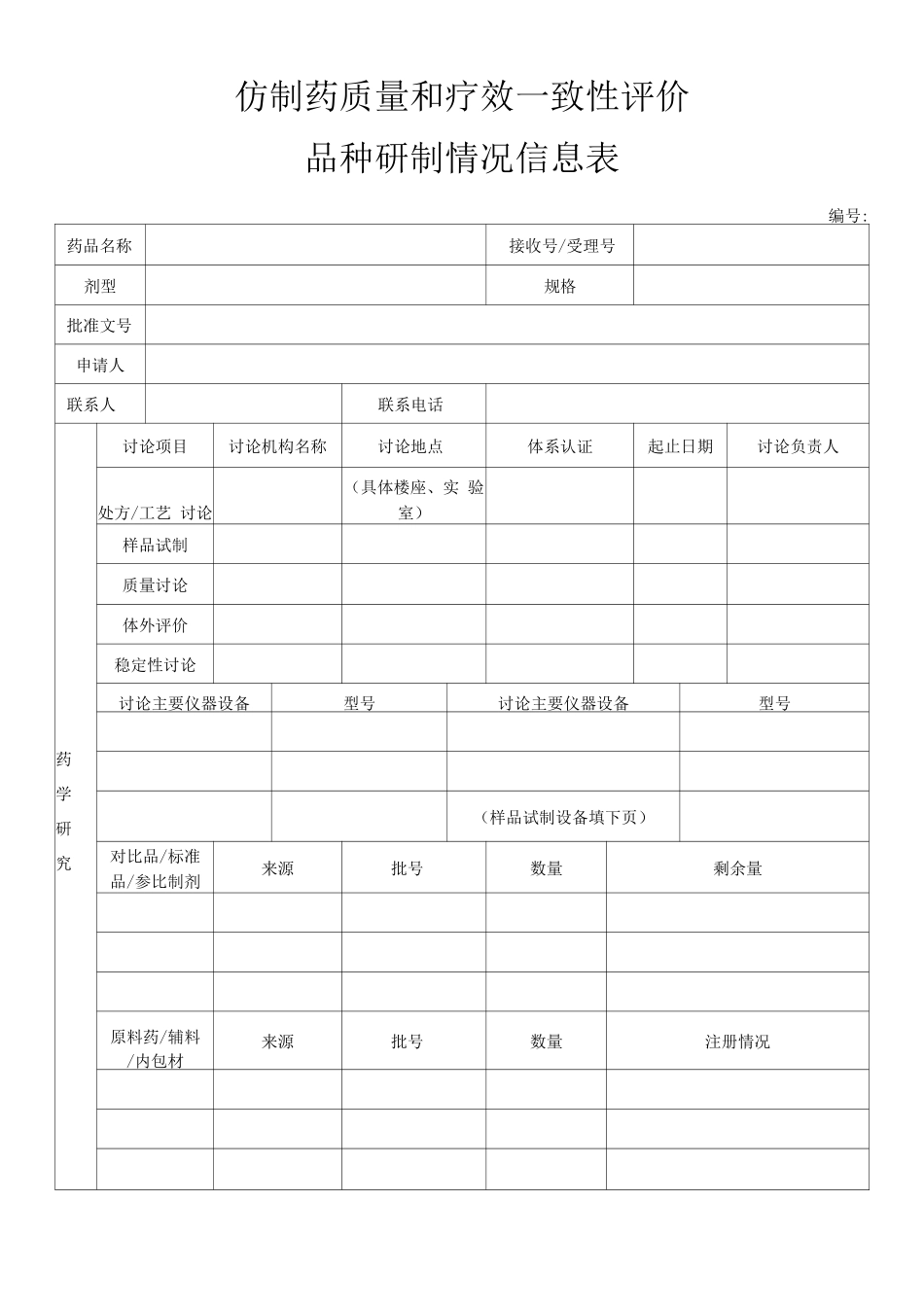
仿制药质量和疗效一致性评价品种研制情况信息表编号:药品名称接收号/受理号剂型规格批准文号申请人联系人联系电话药 学 研 究讨论项目讨论机构名称讨论地点体系认证起止日期讨论负责人处方/工艺 讨论(具体楼座、实 验室)样品试制质量讨论体外评价稳定性讨论讨论主要仪器设备型号讨论主要仪器设备型号(样品试制设备填下页)对比品/标准 品/参比制剂来源批号数量剩余量原料药/辅料/内包材来源批号数量注册情况样品试制批号试制日期用途主药投料量试制量使用量剩余量主要设备试制地点主要设备试制地点(具体楼座、实验室)试制原始记录共页负责人(签名)主要检验仪器检验地点主要检验仪器检验地点(具体楼座、实验室)检验原始记录共页负责人(签名)本报告表中填写内容和所附资料均属实
如查有不实之处,本单位负法律责任,并承担由此造成的 一切后果
申报单位负责人签名:(申请人公章)年 月 日注:本表一式四份,其中三份原件,国家食品药品监督管理总局受理中心存一份原件,其余报送国家食品 药品监督管理总局药品审评中心,药品审评中心根据立卷审查提出有因检查后,将该表原件一份转核查中 心供现场检查