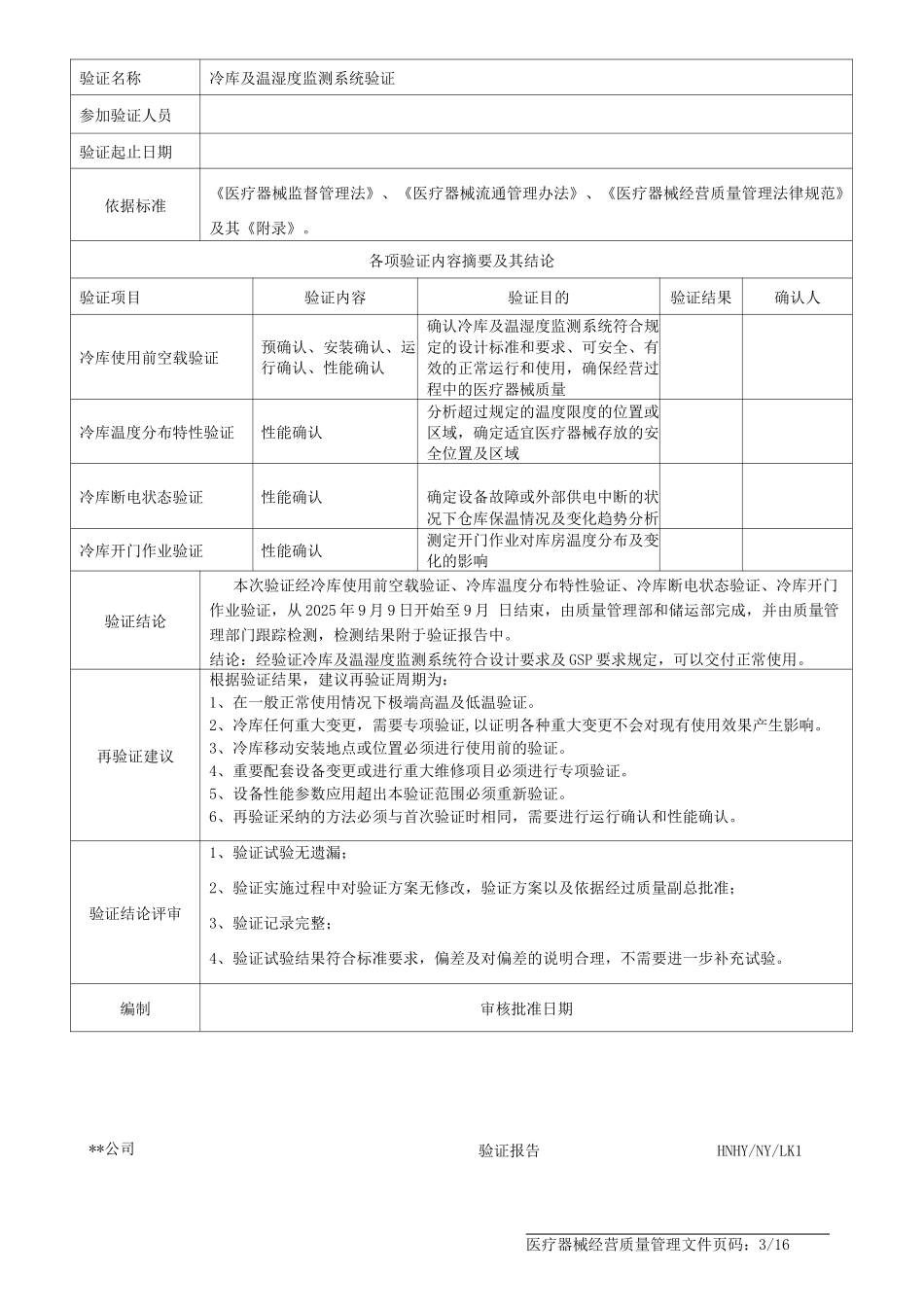
验证报告验证名称:冷库及温湿度监测系统验证项目主持:起止日期:* *公司医疗器械经营质量管理文件页码:1/16**公司验证报告HNHY/NY/LK11、验证报告2、冷库及温湿度监测系统验证方案3、验证小组人员列表4、验证日期进度表5、冷库预确认表6、安装确认所需文件资料7、冷冻机组设备登记8、冷库安装情况检查表9、冷库电器部分检查情况表10、温湿度自动记录仪安装检查情况表11、验证用相关文件确认表12、仪器仪表校验记录13、参加验证人员培训确认表14、冷库制冷系统、操作控制系统功能检查记录表15、偏差及偏差处理记录16、冷库使用前空载验证17、冷库温度分布特性验证18、冷库断电状态验证19、冷库开门作业验证医疗器械经营质量管理文件页码:2/16**公司验证报告HNHY/NY/LK1验证名称冷库及温湿度监测系统验证参加验证人员验证起止日期依据标准《医疗器械监督管理法》、《医疗器械流通管理办法》、《医疗器械经营质量管理法律规范》及其《附录》。各项验证内容摘要及其结论验证项目验证内容验证目的验证结果确认人冷库使用前空载验证预确认、安装确认、运行确认、性能确认确认冷库及温湿度监测系统符合规定的设计标准和要求、可安全、有效的正常运行和使用,确保经营过程中的医疗器械质量冷库温度分布特性验证性能确认分析超过规定的温度限度的位置或区域,确定适宜医疗器械存放的安全位置及区域冷库断电状态验证性能确认确定设备故障或外部供电中断的状况下仓库保温情况及变化趋势分析冷库开门作业验证性能确认测定开门作业对库房温度分布及变化的影响验证结论本次验证经冷库使用前空载验证、冷库温度分布特性验证、冷库断电状态验证、冷库开门作业验证,从 2025 年 9 月 9 日开始至 9 月 日结束,由质量管理部和储运部完成,并由质量管理部门跟踪检测,检测结果附于验证报告中。结论:经验证冷库及温湿度监测系统符合设计要求及 GSP 要求规定,可以交付正常使用。再验证建议根据验证结果,建议再验证周期为:1、在一般正常使用情况下极端高温及低温验证。2、冷库任何重大变更,需要专项验证,以证明各种重大变更不会对现有使用效果产生影响。3、冷库移动安装地点或位置必须进行使用前的验证。4、重要配套设备变更或进行重大维修项目必须进行专项验证。5、设备性能参数应用超出本验证范围必须重新验证。6、再验证采纳的方法必须与首次验证时相同,需要进行运行确认和性能确认。验证结论评审1、验证试验无遗漏;2、验证实施过程中对验证方案...