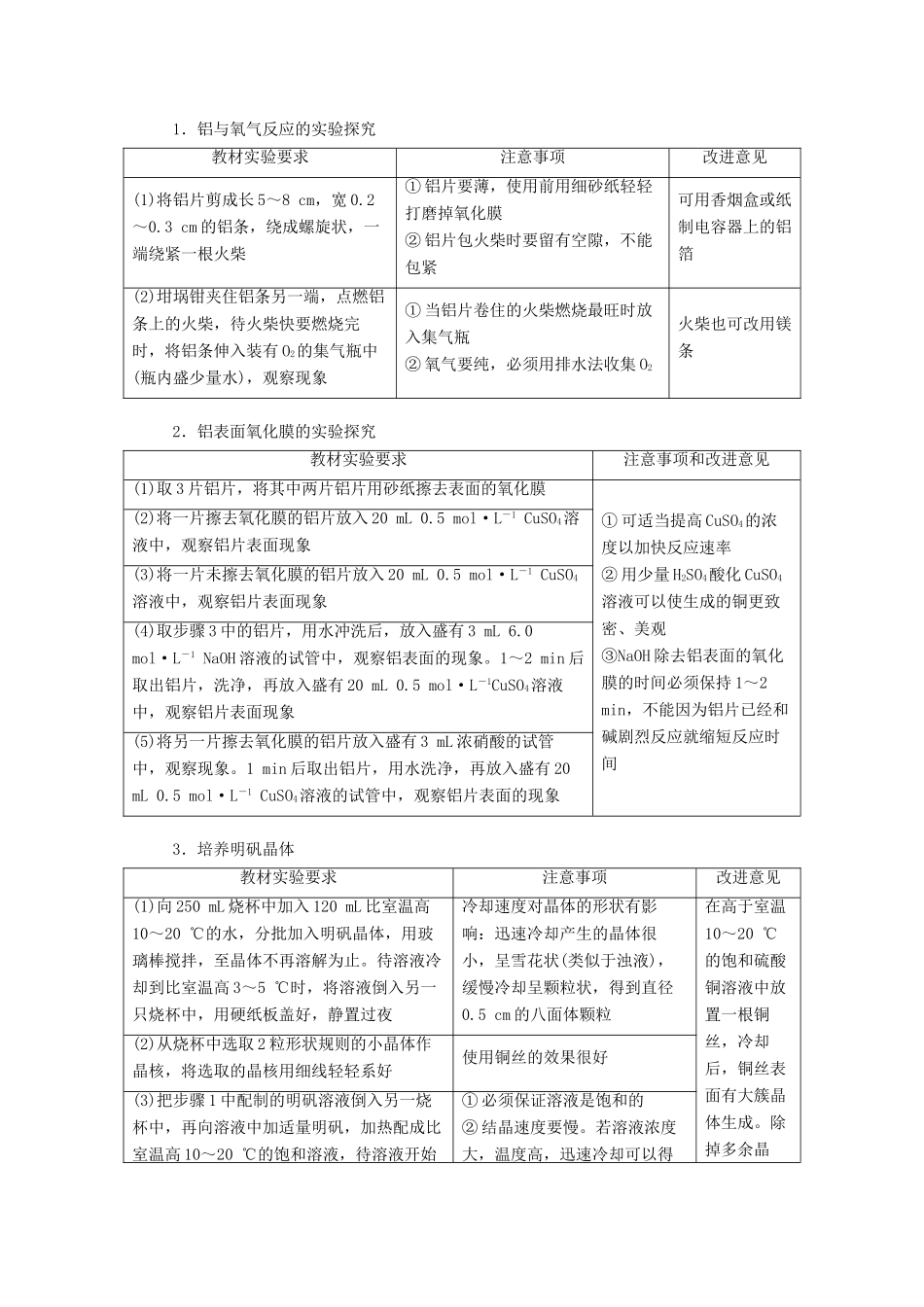
课题 1 铝及其化合物的性质[浙江选考·加试要求]———————————————————————————————————1.铝片(条)燃烧的方法。2.铝表面氧化膜的作用。1.Al3+与 Al(OH)的相互转化Al、Al2O3、Al(OH)3分别与强酸、强碱反应可归纳为――→Al(OH)Al3+――→Al3+与 Al(OH)相互转化关系可归纳为下列关系式 2.配位键和配合物(1)配位键:若甲方具有已配对的孤对电子,乙方具有能量与之相近的空轨道,则成键的两个电子完全由甲方提供,如此所形成的化学键称为配位键。(2)配合物的组成[器材与原理]相关器材 1.以实验巩固铝的化学性质。2.以实验巩固可溶性铝盐的化学性质。3.通过铝及其化合物的学习,培养细致、认真的科学态度。———————实验要素先知道———————实验过程详剖析集气瓶、毛玻璃、烧杯、试管、酒精灯、坩埚钳、镊子、玻璃棒、剪刀、火柴、砂纸、温度计、硬纸板、细线、铁架台。相关原理1.铝的性质(1)原子结构铝的原子结构示意图是。(2)化学性质① 铝在空气中会产生致密的氧化膜,有很好的抗蚀性。② 铝遇冷的强氧化性浓酸,如浓硫酸或浓硝酸,氧化膜加厚而使铝钝化。铝具有相当强的还原性,它与氧的化学亲合力也很强。③ 因为铝既能与稀硫酸或盐酸发生置换反应,又能与苛性钠溶液反应生成氢气与Al(OH),所以铝器不应接触碱或酸,即铝能较好地抗氧而不耐酸、碱。④ 铝跟卤素单质反应,生成对应的卤化铝。如铝粉与碘粉混合后,滴入水作为催化剂,即可发生燃烧。在高温下还能和硫、氮、碳反应生成 Al2S3、AlN 和 Al4C3。铝与硫的粉状混合物点燃,可反应生成硫化铝。这是硫化铝的唯一制法。⑤ 铝具有强还原性,氧化物稳定,生成氧化物时会放出大量的热,而使其他金属氧化物还原并熔化。工业上可用铝冶炼金属 Mn、Co、W、Cr 等,如 Cr2O3+2Al=====2Cr+Al2O3。⑥ 常温下 Al 和水不反应,若和汞生成铝汞齐,则能将水分解产生氢气,铝和酸、碱反应也能产生氢气。2.铝的重要化合物(1)氢氧化铝:白色固体,在溶液中析出时为胶絮状,难溶于水,是典型的两性氢氧化物。用电离平衡观点理解其两性时,可用下式表示:Al(OH)3Al3++3OH-,Al(OH)3+H2OAl(OH)+H+。遇强酸,因中和了 OH - 而使平衡向生成 Al 3 + 的方向移动;遇强碱,因中和了 H+而使平衡向生成 Al(OH)的方向移动。实验室可用适量 NaOH 溶液与铝盐反应制取,但碱稍过量则发生沉淀溶解现象,因此...