CAR—T 细胞治疗质量控制浅谈细胞治疗,将改变人类疾病的治疗范式,由过去重复的症状控制转为一次性的治愈是引领生物医学的希望
其中,嵌合抗原受体(CAR)T 细胞疗法是近年来进展非常迅速的一种细胞治疗技术
目前在全球已有两款药物获得 FDA 的批准上市,分别是诺华的 Kymriah 和凯特的YESCARTA,中国有多家公司产品进入临床申报阶段,这种疗法已成为更多患者的选择,CAR—T 细胞制造过程符合全球监管要求成为广泛讨论的话题
细胞治疗质量控制分析其中细胞质量控制贯穿 CAR—T 从研发到临床的所有步骤,但 CAR-T 作为“活"的药物,其很多特性与传统药物有很大的差别,下表列举了与传统药物的主要差异点:第一个上市的 CAR-T 药物 Kymriah 的释放标准涉及到多个方面的指标,下图是我收集到的 Kymriah 的释放指标所需要测试的实验:KITE 的 YESCARTA 的质量控制也涉及到非常多的生物学实验,篇幅有限,就不一一列举了,具体指标可参考如下的链接:https://www
gov/downloads/BiologicsBloodVaccines/CellularGeneTherapyProducts/ApprovedProducts/UCM584335
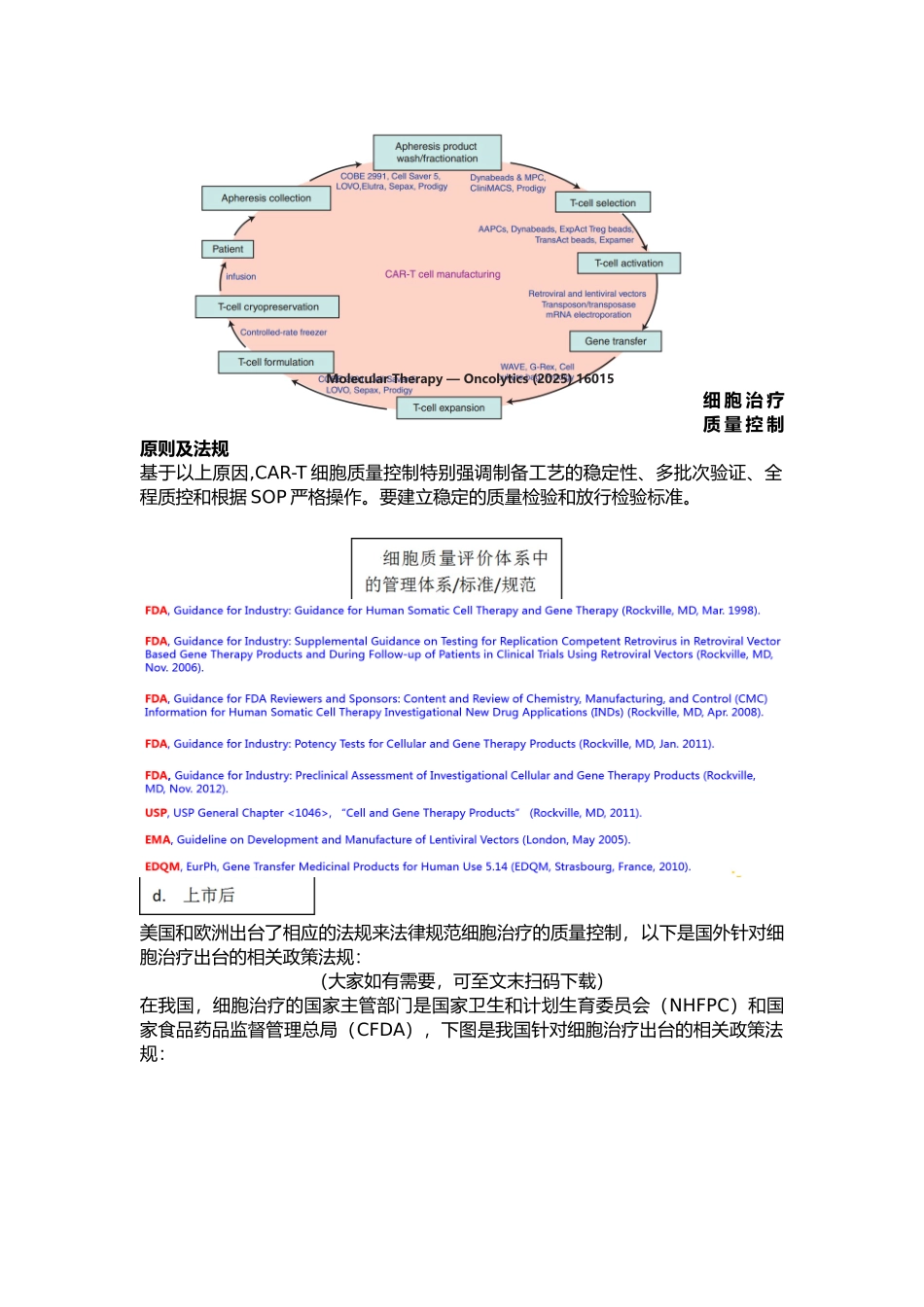
pdf另一方面 CAR-T 制造工艺复杂,下图列举了 CAR-T 的制作流程,其中涉及到病毒转染,外源物质的引进,长时间培育等因素,这势必对质量控制提出了巨大的挑战
细 胞 治 疗质 量 控 制原则及法规基于以上原因,CAR-T 细胞质量控制特别强调制备工艺的稳定性、多批次验证、全程质控和根据 SOP 严格操作
要建立稳定的质量检验和放行检验标准
美国和欧洲出台了相应的法规来法律规范细胞治疗的质量控制,以下是国外针对细胞治疗出台的相关政策法规:(大家如有需要,可至文末扫码下载)在我国,细胞治疗的国家