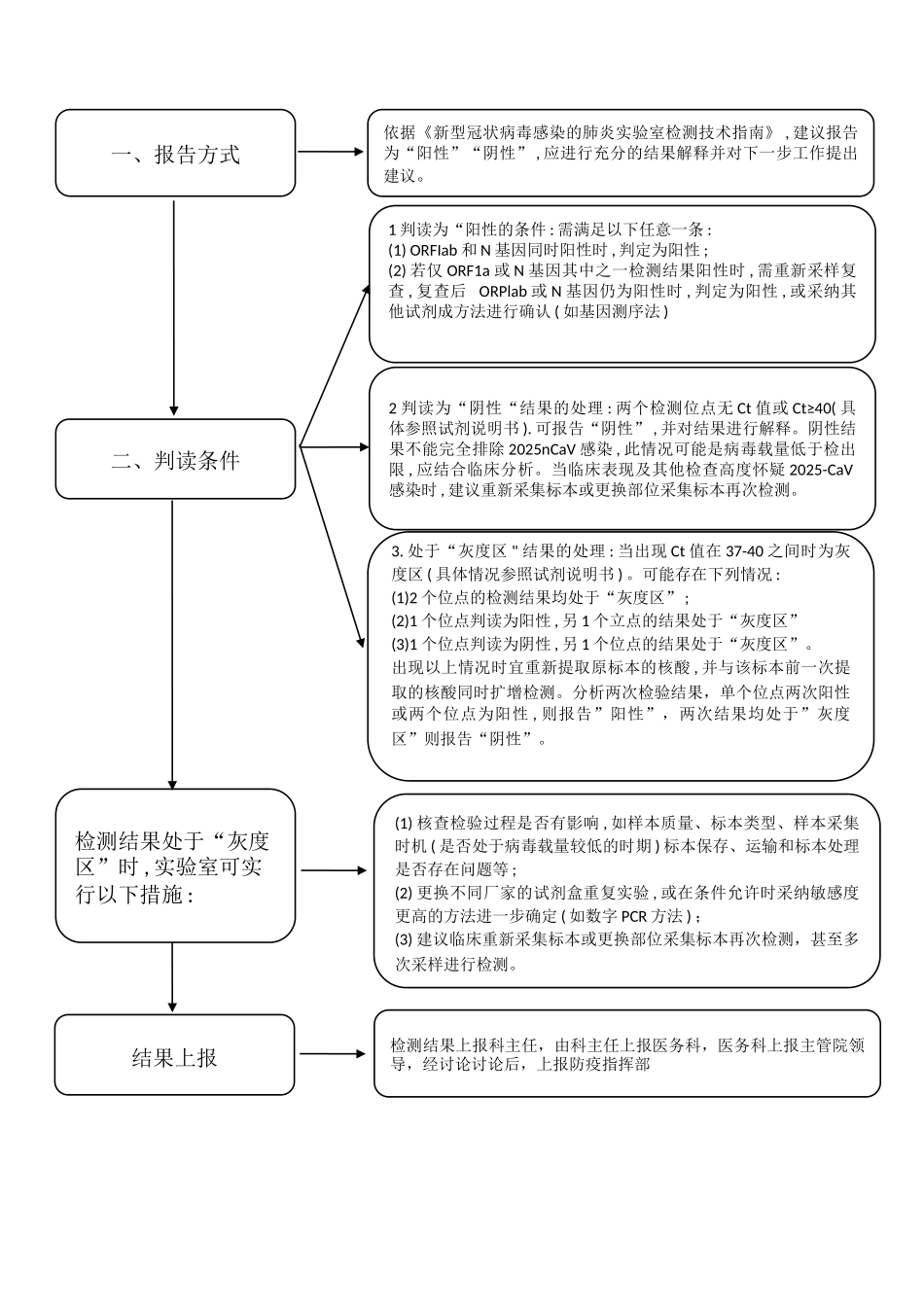
检测结果处于“灰度区”时 , 实验室可实行以下措施 :一、报告方式二、判读条件依据《新型冠状病毒感染的肺炎实验室检测技术指南》 , 建议报告为“阳性”“阴性” , 应进行充分的结果解释并对下一步工作提出建议
1 判读为“阳性的条件 : 需满足以下任意一条 :(1) ORFIab 和 N 基因同时阳性时 , 判定为阳性 ;(2) 若仅 ORF1a 或 N 基因其中之一检测结果阳性时 , 需重新采样复查 , 复查后 ORPlab 或 N 基因仍为阳性时 , 判定为阳性 , 或采纳其他试剂成方法进行确认 ( 如基因测序法 )2 判读为“阴性“结果的处理 : 两个检测位点无 Ct 值或 Ct≥40( 具体参照试剂说明书 )
可报告“阴性” , 并对结果进行解释
阴性结果不能完全排除 2025nCaV 感染 , 此情况可能是病毒载量低于检出限 , 应结合临床分析
当临床表现及其他检查高度怀疑 2025-CaV感染时 , 建议重新采集标本或更换部位采集标本再次检测
处于“灰度区 " 结果的处理 : 当出现 Ct 值在 37-40 之间时为灰度区 ( 具体情况参照试剂说明书 )
可能存在下列情况 :(1)2 个位点的检测结果均处于“灰度区” ;(2)1 个位点判读为阳性 , 另 1 个立点的结果处于“灰度区”(3)1 个位点判读为阴性 , 另 1 个位点的结果处于“灰度区”
出现以上情况时宜重新提取原标本的核酸 , 并与该标本前一次提取的核酸同时扩增检测
分析两次检验结果,单个位点两次阳性或两个位点为阳性 , 则报告”阳性”,两次结果均处于”灰度区”则报告“阴性”
(1) 核查检验过程是否有影响 , 如样本质量、标本类型、样本采集时机 ( 是否处于病毒载量较低的时期 ) 标本保存、运输和标本处理是否存在问题等 ;(2) 更换不同厂家的试剂盒重复实验 , 或在条件允许时采纳敏感度