附件 1:编号:医 疗 器 械 产 品 分 类 界 定 申 请 表产品名称:申请企业:国家食品药品监督管理局医疗器械标准管理中心制填 表 说 明1.本申请表应打印
填写内容应完整、清楚、干净,不得涂改
2.本申请表可从如下 www
cn 或 www
nicpbp
cn 免费下载
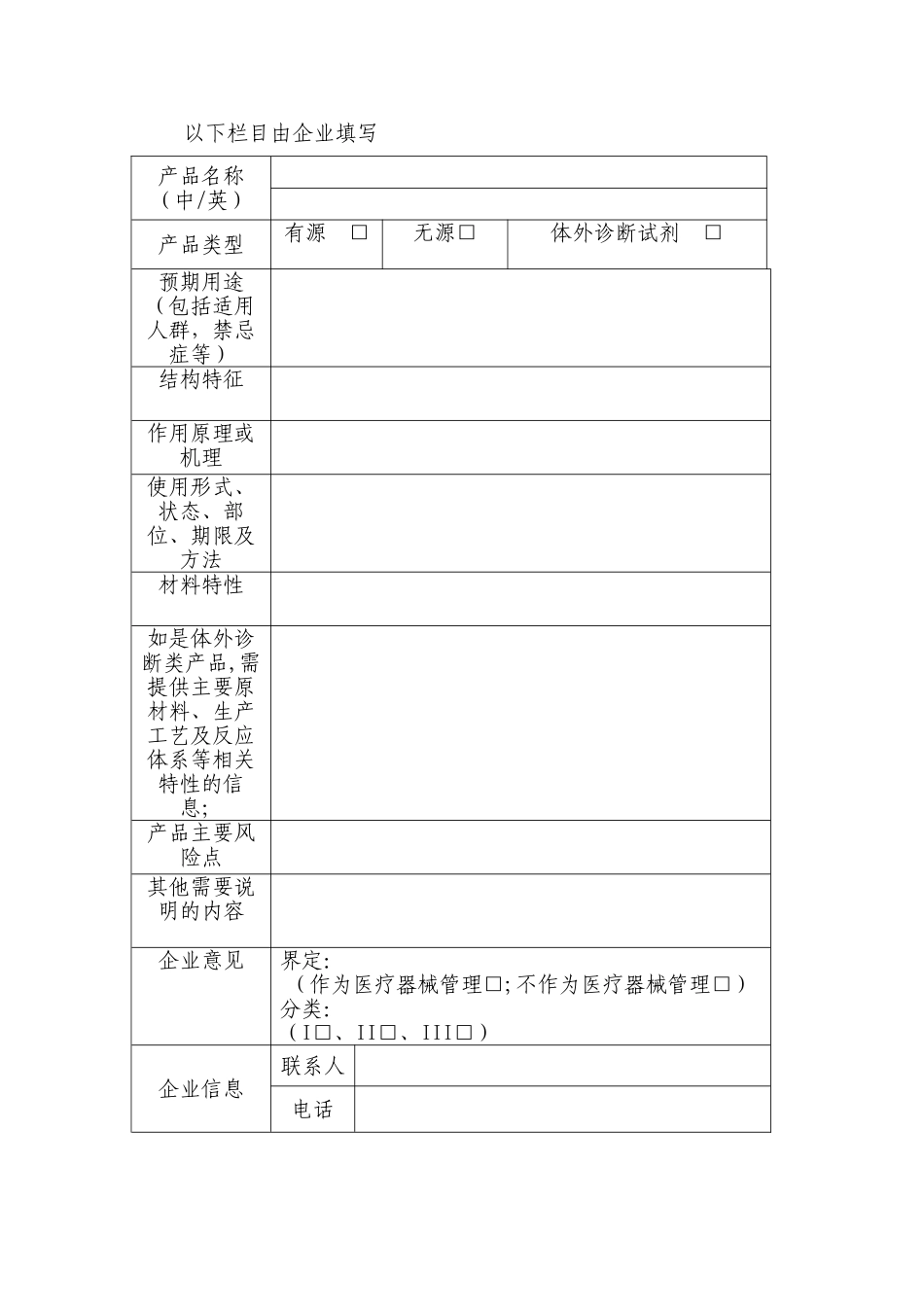
以下栏目由企业填写 产品名称(中/英)产品类型有源 □无源□ 体外诊断试剂 □预期用途(包括适用人群,禁忌症等)结构特征作用原理或机理使用形式、状态、部位、期限及方法材料特性如是体外诊断类产品,需提供主要原材料、生产工艺及反应体系等相关特性的信息;产品主要风险点其他需要说明的内容企业意见界定:(作为医疗器械管理□;不作为医疗器械管理□)分类:(I□、II□、III□)企业信息联系人电话地址(邮编)电子信箱传真签字(盖章)省级食品药品监督管理部门意见分类界定意见:界定:(作为医疗器械管理□;不作为医疗器械管理□)分类:(I□、II□、III□)签字(盖章)注:境外及台、港、澳企业无需填写“省级食品药品监督管理部门意见”一栏
如填写内容可另附页