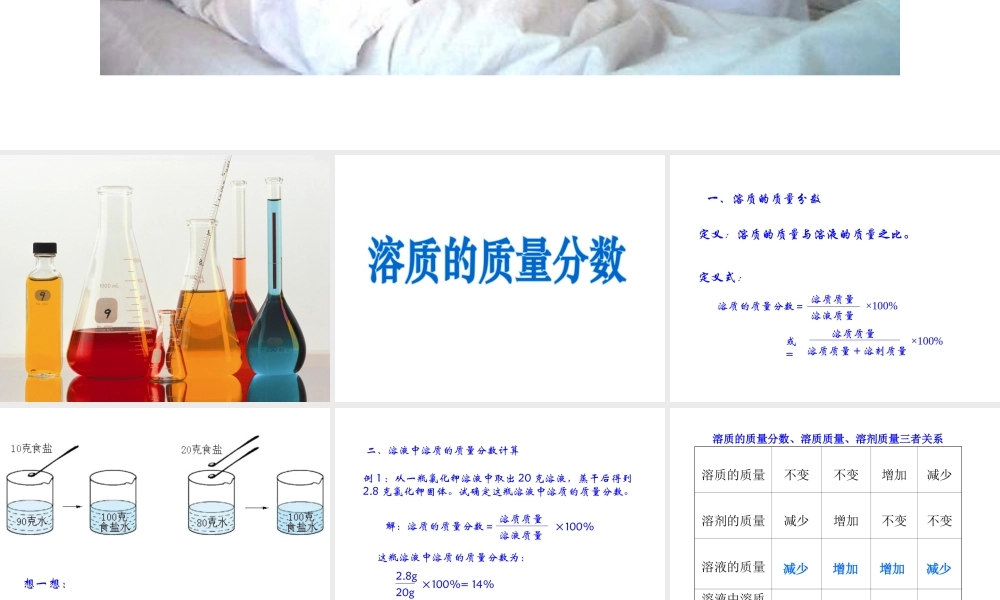
一、溶质的质量分数溶质质量溶液质量×100%溶质的质量分数=或=溶质质量溶质质量 + 溶剂质量×100%定义式:定义:溶质的质量与溶液的质量之比
想一想:上述实验配制的溶液中氯化钠的质量分数是多少
二、溶液中溶质的质量分数计算 例 1 :从一瓶氯化钾溶液中取出 20 克溶液,蒸干后得到2
8 克氯化钾固体
试确定这瓶溶液中溶质的质量分数
这瓶溶液中溶质的质量分数为:溶质质量溶液质量×100%解:溶质的质量分数=答:这瓶溶液中氯化钾的质量分数为 14%
8g20g ×100%= 14%溶质的质量不变不变增加减少溶剂的质量减少增加不变不变溶液的质量溶液中溶质的质量分数减少增加减少减少减少增加增加增加溶质的质量分数、溶质质量、溶剂质量三者关系例 2 :配制 500mL20% 的硫酸需要 98% 的硫酸多少毫升
解:查硫酸密度和溶质质量分数对照表得出: 20% 的硫酸的密度为 1
14g/cm3 , 98% 的硫酸的密度为 1
84g/cm3
设:需 98% 的硫酸的体积为 x
根据:质量 = 体积 × 密度500 cm3 × 1
14g/cm3 × 20%稀释后溶液质量 =500cm3 ×1
14g/cm3 x = 63
2 cm3答:配制 500mL20% 的硫酸需要 63
2mL98% 的硫酸
稀释前溶液质量 = x × 1
84g/cm3 稀释前溶液中 H2SO4 质量稀释后溶液中含 H2SO4 的质量=因被稀释的溶液里溶质的质量在稀释前后不变x × 1
84g/cm3 × 98%比较项目 溶解度 溶质的质量分数 意义 温度要求 溶剂量要求 溶液是否饱和 单位 关系式 克溶剂质量溶质质量溶解度100%100溶液质量溶质质量溶质的质量分数溶解度与溶质的质量分数的比较表示物质溶解性的度量,受外界温度、压强等影响表示溶液中溶质质量的多少,不受外界条件限制